News Detail
 来源:本站
来源:本站
 浏览量:18490
浏览量:18490
药物代谢,也称为药物的生物转化,是药物从体内消除的主要方式之一,代谢过程通常由一系列酶促反应来完成。与药物代谢关系最大的是细胞色素CYP450(Cytochrome P450 proteins, CYP)酶系,它主要存在于人体肝脏中,在肾脏,小肠,肺,脑中也有少量表达,参与生物体许多内源性和外源性物质(包括大多数临床药物)的生物转化。
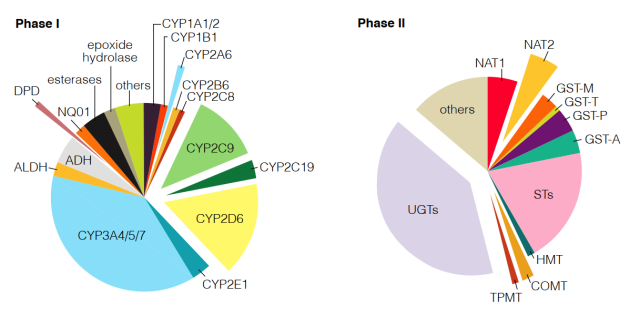
Polymorphic drug-metabolizing enzymes
细胞色素酶是一种以铁卟啉为辅基的蛋白质(cytochrome protein),又称混合功能氧化酶、单加氧酶,因其还原型与CO的复合物在450 nm处有一强吸收峰,故而得名细胞色素P450.CYP是一个基因超家族,参与编码500多种酶蛋白。根据这些基因所编码蛋白质的相似程度,将其划分为不同的基因家族和亚家族。常见的命名如CYP2D6.2表示家族,D表示亚家族,6表示某种特定的酶个体。其中CYP1A2、CYP2C9、CYP2C19、CYP2D6、CYP2E1和CYP3A4是CYP450最主要的6种亚型,其含量约占肝脏内CYP450酶总量的80%,其中CYP3A4在多数人群中占人体总CYP的50%,且90%的药物均由这6种亚型代谢。在已明确的药物相互作用中,CYP450酶系引起的药物相互作用占70%。因此了解每一个CYP所催化的药物类型,对于在临床上合理用药,避免药物的不良反应,个体化给药方案的实施以及阐明在代谢环节上发生的药物相互作用很有意义。
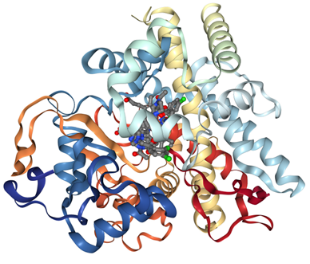
Crystal structure of human P450 3A4 in complex with ketoconazole
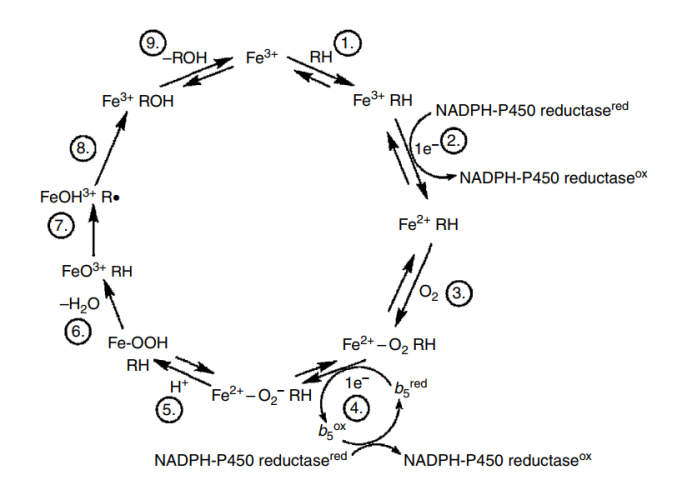
Mechanism of catalytic cycle for CYP450 reactions
人类和动物体内细胞色素P450酶类与肝病和癌症等诸多疾病相关,人们希望通过深入研究CYP450的功能,为不久的将来能战胜肝病、癌症和其他疾病提供可能性。CYP450酶具有遗传多态性,导致药物代谢存在着种族和个体差异。这种特性在CYP2C19和2D6两个亚型上表现的尤其明显,举个例子:质子泵抑制剂奥美拉唑(CYP2C19底物)在日本人群中不良反应较多,很大原因就是日本人中约有五分之一为慢代谢型(poor metabolizer, PM),而快代谢型(extensive metabolizer, EM)与PM的血药浓度相差约7倍之多。此外,CYP450酶底物结构的特异性不强,选择性低,不同亚型CYP能催化同一底物,而多种底物可被同一种CYP所代谢,且其活性容易受遗传因素、年龄、性别、营养状况、疾病状态、环境等多种因素影响。胎儿、新生儿和老人的用药尤其需要注意,胎儿和新生儿的CYP系统尚未发育完全,老年人肝血流降低、CYP活性降低,这类人群的用药种类和剂量应特别关注,否则易引起不良反应和毒性。
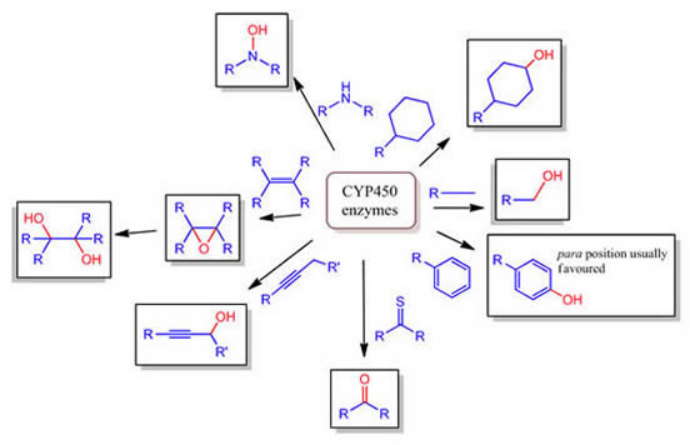
The CYP450 enzymes related small subset of reactions
临床用药要考虑药物药物相互作用(Drug-drug interaction,DDI),主要是因为环境中有很多化学物质可使CYP活性增强(诱导剂)或者减弱(抑制剂),改变药物代谢速度,影响药物的作用效果。
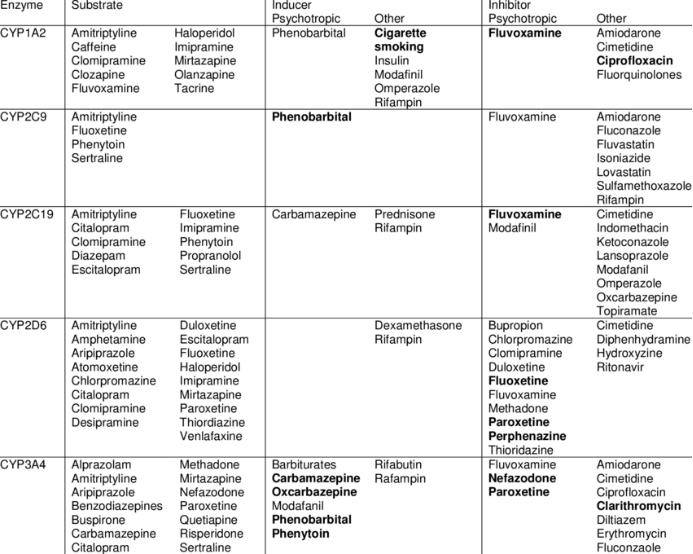
CYP450 Enzymes Commonly Involved in Drug Interactions
CYP酶被诱导后可加快自身或者其他药物的代谢,血药浓度降低,连续用药使药效降低,降低治疗效果,如苯巴比妥和华法林连用时,可使华法林的抗凝效果减弱;但对于某些在体内活化或产生代谢毒性化合物的药物来讲,酶诱导后会导致疗效增强和毒性反应,这个在日常生活中就可以很好体现,乙醇是肝CYP2E1的诱导剂,长期饮酒后,被乙醇诱导的CYP2E1能使对乙酰氨基酚转化的毒性代谢物增多,诱发肝毒性。菠菜等因蔬菜富含吲哚类物质,诱导小肠CYP3A的表达,使非那西丁等药物首关效应增强,血药浓度减少,降低疗效;服用降压药硝苯地平的患者不能同时进食柚子等水果,原因就是葡萄柚汁中含生物类黄酮及柚苷,能抑制肝脏及小肠CYP3A活性,使药物的首过效应减少,血药浓度增加,易导致中毒反应。
CYP酶被抑制后也会产生治疗效果减弱或增强甚至毒性的效果:比如在体内活化的药物,如可待因,其CYP2D6代谢产物吗啡具有镇痛作用,与该酶抑制剂合用后,活性代谢物吗啡生成量减少,降低了作用效果;在体内灭活的药物,如CYP3A4底物特非那定,与抑制剂合用时,代谢速度降低,血药浓度显著增加,可诱发心律失常的不良反应。
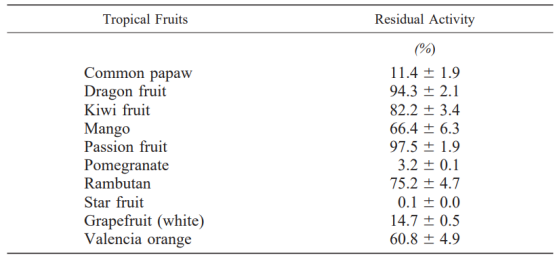
Effects of components contained in tropical fruits on midazolam 1-hydroxylase activity of human liver microsomes
在药物研发阶段,确定化合物在体内代谢的速度和代谢酶的亚型,并对CYP抑制和诱导作用进行评价,可预估化合物存在的潜在安全性问题,通过对主要代谢产物结构的研究,可以指导化合物的结构修饰,提高代谢稳定性。当然,药物代谢酶还有很多其他类型,本文暂不涉及。
药物代谢的研究方法,体外研究和体内研究相辅相成。体外研究,可实现高通量筛选,对大量的候选化合物进行初筛,初步评价药动学特性,缩小体内筛选的范围。体内研究可以对体外研究的结果加以验证并帮助寻找更富预见性体外代谢模型。
体外代谢研究——体外代谢研究选择性强,可以排除体内诸多的干扰因素,具有快速简便的特点,且不需要大量动物,因此研究费用相对较低。体外研究多停留在肝微粒体、肝细胞、重组酶等代谢体系中。常用的体外代谢研究方法有:肝微粒体体外温孵法、重组P450酶体外温孵法、肝细胞体外温孵育法、离体肝灌流法、肝切片法以及“cocktail”探针法。
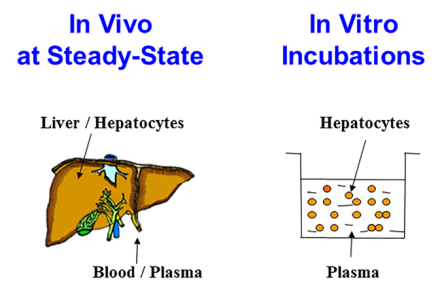
In vitro model of HHEP suspended in human plasma and comparison to an in vivo model
肝微粒体体外温孵法,已广泛应用于预测药物体内代谢清除等方面的研究,在体外模拟生理环境条件进行代谢反应,利用液质联用仪测定温孵液中原型药物和代谢产物的含量,并对代谢产物进行初步的分析和鉴定,研究代谢产物的结构和代谢途径。通过测定药物体外代谢酶促反应动力学参数Vmax和Km,不同性别和种属的微粒体代谢稳定性差异,来预测药物的体内代谢清除率、对药酶的抑制作用、药物代谢的种属和性别差异、药物的代谢相互作用等方面的研究。CYP450抑制是产生DDI的主要原因之一。《FDA关于药物相互作用研究指南》中指出:在新药开发阶段,新药的代谢特征及其与其他药物的相互作用应该尽可能早地提出与探讨,这些数据将成为评价新药安全性和有效性的参考。
爱思益普DMPK团队目前已经拥有常规CYP450活性分析实验,可以使用重组蛋白、微粒体、肝细胞、组织裂解样本等材料,提供CYP450活性分析实验,部分结果如下显示:
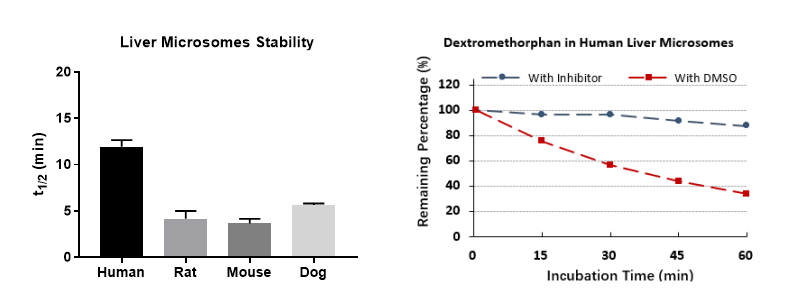
Liver microsomes stability (ICE data)
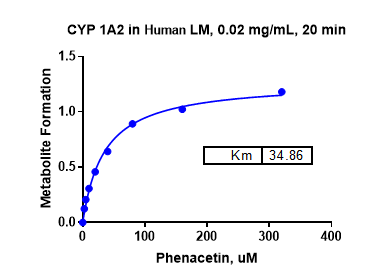
Km determination, CYP1A2 in Human (ICE data)
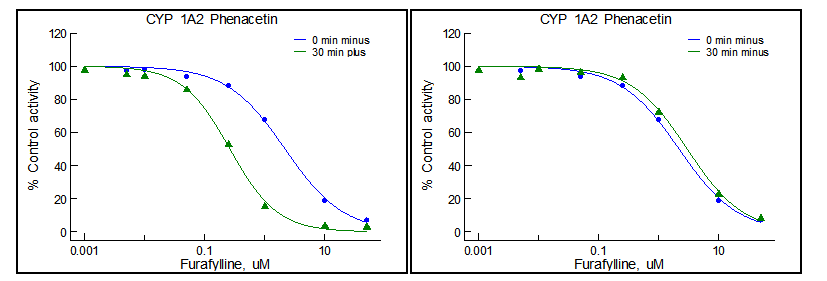
CYP 1A2 Time Dependent Inhibition in Human Liver Microsomes (ICE data)
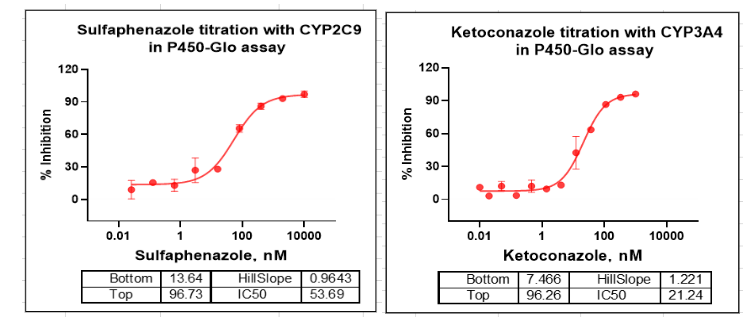
P450 Glo assay using recombinant protein (ICE data)
体内代谢研究——一般在动物体进行,体内药动学除受代谢影响外,易受吸收、分布和排泄过程的影响,这种方法需要时间和人力较多,消耗实验动物和分析大量的样品,研究费用也相对高昂。爱思益普团队可以提供快速PK及MetID分析,便于项目开展所需要的化合物在体内代谢研究。
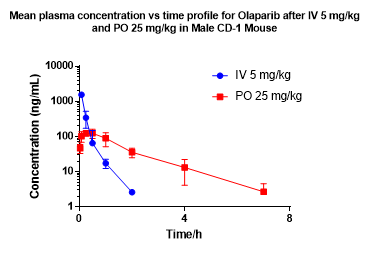
Concentration vs time profile of Olaparib (ICE data)
在新药的开发研究阶段应了解何种肝药酶参与了药物代谢及其本身对肝药酶的影响,对于那些治疗指数小又常与其他药物合用的药物这一点尤为重要。这一方面的工作可以为新药的临床研究和临床的合理用药提供理论依据。
爱思益普DMPK团队,建立了系列和药物代谢相关的体外和体内实验,包括药物肝微粒体代谢稳定性、CYP450酶抑制、TDI和Met ID等体外实验,还包括大小鼠及犬的静脉注射、口服给药、腹腔注射和皮下注射等体内实验,能够结合体外酶学、细胞学实验优化平台,提供定制化的体内外实验,很好的为客户提供药代动力学服务。
结合早期靶点验证与机理研究的平台、酶学和细胞学的筛选平台、成药性评价的ADMET平台、PK/PD的分析平台、谱学筛选平台(kinase panel, safety panel, cell panel, etc.)等,爱思益普可以更好更快地为药物研发的团队高效地提供药物构效关系测试,加速中国新药研发项目的进程。
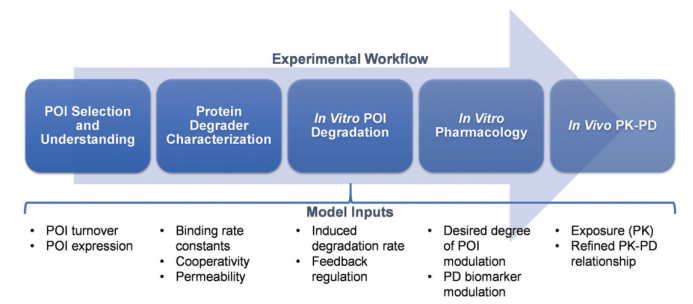
A proposed translational PK–PD roadmap for protein degrader therapeutics
参考文献
1.Drug Interactions and Polypharmacy - Scientific Figure on ResearchGate. Available from: https://www.researchgate.net/figure/CYP450-Enzymes-Commonly-Involved-in-Drug-Interactions_tbl3_289088073
2.Hidaka M, Fujita K, Ogikubo T, Yamasaki K, Iwakiri T, Okumura M, Kodama H, Arimori K. Potent inhibition by star fruit of human cytochrome P450 3A (CYP3A) activity. Drug Metab Dispos. 2004 Jun;32(6):581-3. doi: 10.1124/dmd.32.6.581. PMID: 15155547.
3.Kerns, E. H. and L. Di (2008). Drug-like Properties: Concepts, Structure Design and Methods: from ADME to Toxicity Optimization, Elsevier Inc.
4.Lu, C, Di, L. In vitro and in vivo methods to assess pharmacokinetic drug– drug interactions in drug discovery and development. Biopharm Drug Dispos. 2020; 41: 3– 31. https://doi.org/10.1002/bdd.2212
5.Evans WE, Relling MV. Pharmacogenomics: translating functional genomics into rational therapeutics. Science. 1999 Oct 15;286(5439):487-91. doi: 10.1126/science.286.5439.487. PMID: 10521338.
6.刘晓强,袁淋文,臧敏,曹云,王丹,杨劲,孔毅.评价HPPH对细胞色素P450酶体外代谢活性的影响[J].药学与临床研究,2014.22(1):29-33
7.王广基, 刘晓东, 柳晓泉. 药物代谢动力学[M]. 化学工业出版社, 2005.
8.Bartlett, D. W. and A. M. Gilbert (2022). Chem Soc Rev 51(9): 3477-3486.
地址:北京市通州区科创十三街与经海路交汇处
电话:010-67809840
邮箱:services@ice-biosci.com
官网:http://www.ice-biosci.com/

扫一扫关注
爱思益普公众号


业务咨询
北京
业务咨询专线:010-6780-9840
联系地址:北京市经济技术开发区科创十三街18号院锋创科技园16号楼
上海
业务咨询专线:010-6780-9840
联系地址:上海市浦东新区蔡伦路780号新技术推广大楼3E5O室
徐州
业务咨询专线:010-6780-9840
联系地址:江苏省徐州市云龙区淮海文博园 二号楼2层
贵州
业务咨询专线:010-6780-9840
联系地址:贵州省贵阳市南明区龙岭路50号 欧美医药产业园一期2号楼



