News Detail
 来源:2024-06-18 09:33:03
来源:2024-06-18 09:33:03
 浏览量:20598
浏览量:20598
慢性粒细胞白血病(chronicmyelogenousleukemia,CML)是一种骨髓增殖性肿瘤,主要由BCR-ABL1融合基因编码的具有持续酪氨酸激酶活性的BCR-ABL1蛋白所致。酪氨酸激酶抑制剂(tyrosinekinaseinhibitor,TKI)可抑制BCR-ABL1的激酶活性,通过TKI治疗达到持续缓解的CML患者生存期显著延长。BCR-ABL1结构域上的某些点突变可导致伊马替尼耐药,第二代、第三代TKI对大多数伊马替尼治疗失败的患者具有良好效果。最新研究发现,无论患者是否存在激酶突变,均有可能发生耐药,提示其他耐药机制的存在,即BCR-ABL1依赖性和BCR-ABL1非依赖性耐药机制,共同参与了耐药的产生,这种情况多见于CML加速期和BCR-ABL1阳性的急性淋巴细胞白血病。
慢性粒细胞白血病(CML)是起源于造血干细胞的一种恶性疾病,也是一种常见的白血病,其发病率居白血病的第3位,约有60%~70%的患者最终死于慢性粒细胞病变。1960年,Nowell和Hauger-foro首次发现CML的发病原因主要体现在其细胞遗传性标志:变异的PH染色体(费城染色体),即ABL(位于9q34的原癌基因)与BCR(位于22q11的基因)发生重组,重组后形成的BCR-ABL融合基因与CML的发病紧密相关,这种变异被认为是CML的始动突变。CML的遗传学特征就是PH染色体的突变,见于90%~95%的CML病例之中,P210是其主要的编码蛋白。P210蛋白与ABL蛋白比酪氨酸激酶活性更强,会减弱细胞对凋亡信号的反应,促进细胞分裂,从而引起白血病。因此,被激活的ABL原癌基因产生了BCR-ABL融合蛋白,其具有更强的酪氨酸激酶活性,使细胞的信号传导异常,导致细胞变异,而重组形成的BCR-ABL融合基因激活了ABL原癌基因。国内外很早便开始关注和研究CML的治疗,传统的治疗方案是以化疗、干扰素治疗为主,但其疗效不甚理想且不良反应较大。而后发现异基因骨髓移植可以治愈CML,然而大部分患者因年龄过大或欠缺供体干细胞而无法进行骨髓移植,且治疗费用昂贵。靶向治疗药物的问世给CML患者带来希望。所谓靶向治疗药物即为对正常细胞的侵害较轻而对微恶性肿瘤的异常分子机制或异常血管的生成等发挥作用的药物。BCR-ABL是治疗CML的药物靶标,BCR-ABL激酶抑制剂便成CML治疗的重要药物,由最开始少数人研究批准上市定义为孤儿药,现已成为国内外研究的热点。
第1代BCR-ABL酪氨酸激酶抑制剂伊马替尼(Imatinib)被认为是第1代酪氨酸激酶抑制剂,由诺华公司开发于2001年获FDA批准上市。激酶的活性环磷酸化方式不同会分别转变成活性或非活性构象。伊马替尼具有特异性是因为其能识别ABL蛋白激酶在非活化状态下的独特构象并选择性的结合。伊马替尼的选择性是其识别ABL激酶与底物结合的保守序列处并与之结合,只对ABL蛋白酪氨酸激酶和其他少数的激酶有抑制活性。
第2代BCR-ABL酪氨酸激酶抑制剂尼洛替尼、拉多替尼、氟马替尼是选择性BCR-ABL酪氨酸激酶抑制剂,达沙替尼、博舒替尼是双重ABL-SRC激酶抑制剂,它们被统称为第2代BCR-ABL酪氨酸激酶抑制剂。尼洛替尼于的细胞抑制活性是伊马替尼的20倍。拉多替尼于的IC50为34nM。氟马替尼于2019年11月在我国批准上市,国内首款批准上市的第2代BCR-ABL抑制剂药物,能够改善部分伊马替尼耐药患者的临床治疗效果,安全性、耐受性良好,对野生型和伊马替尼耐药的患者疗效都强于伊马替尼。达沙替尼于2009年5月被FDA批准上市,用于治疗CML、对包括伊马替尼在内的治疗方案耐药或不能耐受的CML、费城染色体阳性急性淋巴细胞白血病和实体瘤患者的进行治疗。博舒替尼于2012年9月获FDA批准,用于治疗CML。第2代BCR-ABL激酶抑制剂主要针对伊马替尼耐药的突变型BCR-ABL,并同时出现了作用于多靶点的治疗CML的抑制剂,但这些都无法对T315I突变型BCR-ABL激酶起效。
第3代BCR-ABL酪氨酸激酶抑制剂普纳替尼是第3代BCR-ABL酪氨酸激酶抑制剂。由Ariad制药公司研制于2012年12月被美国FDA特许经过快速审批上市,用于ABLT315I突变的CML或Ph+的ALL的治疗,也可用于对以往TKI耐药或不耐受的CML或ALL的治疗。普纳替尼最大的优势是可作用于T315I突变型,使T315I突变型的患者能够得到有效的治疗。
第4代BCR-ABL酪氨酸激酶抑制剂Asciminib是与BCR-ABL1蛋白的肉豆蔻酰位点相结合的别构抑制剂,由是诺华研制的第4代BCR-ABL酪氨酸激酶抑制剂,目前3期临床试验成功,与已批准的ABL1激酶抑制剂不同,它不与激酶的ATP结合位点相结合,而是与激酶结构域中一个位点的空口袋相结合,而该口袋正常情况下是由ABL1肉豆蔻酰化N-末端占据。通过结合肉豆蔻酰位点,该药物可模拟肉豆蔻酸盐的作用,恢复对激酶活性的抑制。由于肉豆蔻酰口袋的独特构象,Asciminib仅对ABL1具有高选择性,并且同时靶向作用于天然和突变的BCR-ABL1包括T315I突变体。
随着CML发病率不断增长,BCR-ABL酪氨酸激酶抑制剂的需求也会越来越大。从靶向药物伊马替尼的上市,肿瘤治疗迎来了靶向治疗时代。但因药物长期使用,部分患者出现了耐药性。随之研发产生了第2代,它们对于野生型和绝大多数突变型都有着超越第1代的抑制作用,但对于T315I突变型依然没有效果。普纳替尼为代表的第3代可以抑制T315I突变型,但因选择性较差,产生脱靶效应,导致了更多的不良反应。Asciminib作为第4代是BCR-ABL1变构抑制剂,可以用于治疗对正构抑制剂耐药或不耐受的CML患者,而且Asciminib联合伊马替尼使用显示了很好的初步疗效,具有良好的安全性及耐受性。因此新型的BCR-ABL酪氨酸激酶抑制剂在提高抑制效果的同时,也应该重视减少不良反应。相信未来会出现更多的抑制剂在抑制野生型和突变型同时,也具有更好的疗效和安全性。激酶谱筛选可以完成早期筛选的问题。
激酶谱筛选的优势:
l提供激酶谱定制服务
l功能性筛选。
l所有靶点均为人源靶点。
l周周安排检测。
l提供中英文报告,可视化结果展示,全面支持中美IND申报。
l更好的售后服务体验,根据客户投稿要求进行展示图的格式修改。
推出的激酶谱类型:
lCDK激酶谱
lTK酪氨酸激酶谱
l80核心野生型激酶谱
l217野生型激酶谱
l330野生型激酶谱
l416全激酶谱
l定制谱
验证数据展示
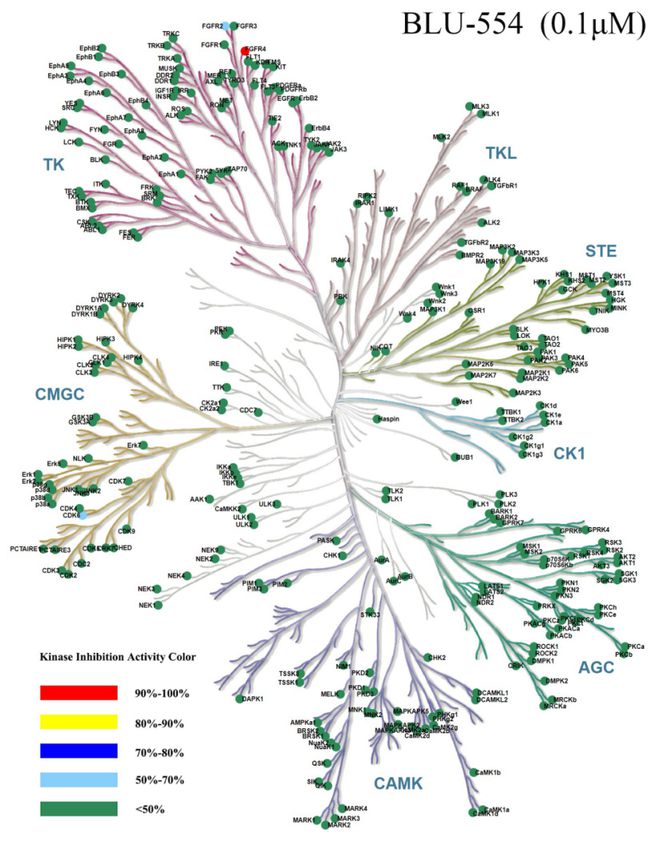
图1KinasePanel416激酶谱树图展示
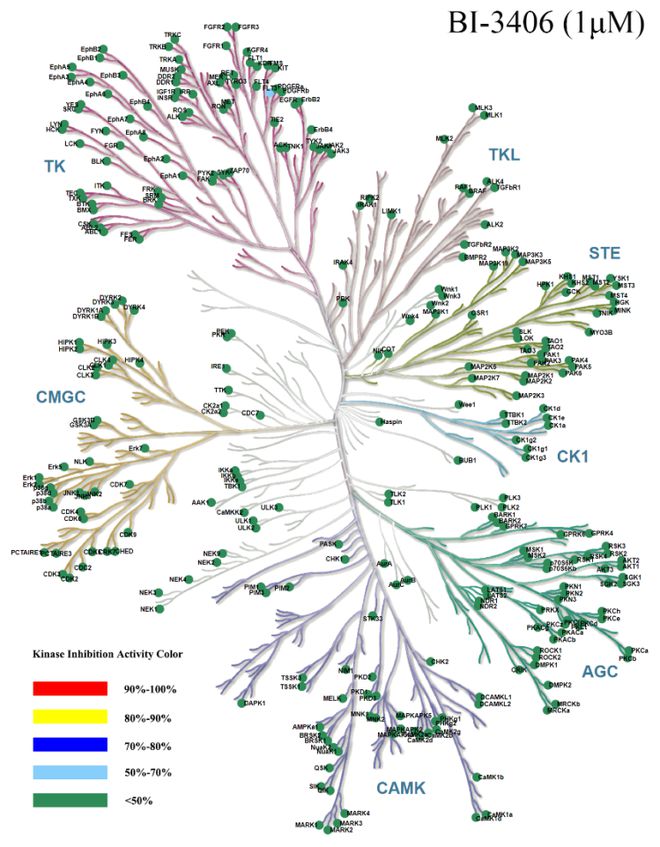
图2KinasePanel416激酶谱树图展示

扫一扫关注
爱思益普公众号


业务咨询
北京
业务咨询专线:010-6780-9840
联系地址:北京市经济技术开发区科创十三街18号院锋创科技园16号楼
上海
业务咨询专线:010-6780-9840
联系地址:上海市浦东新区蔡伦路780号新技术推广大楼3E5O室
徐州
业务咨询专线:010-6780-9840
联系地址:江苏省徐州市云龙区淮海文博园 二号楼2层
贵州
业务咨询专线:010-6780-9840
联系地址:贵州省贵阳市南明区龙岭路50号 欧美医药产业园一期2号楼



