News Detail
 来源:2026-04-01 09:32:41
来源:2026-04-01 09:32:41
 浏览量:11735
浏览量:11735
一、行业背景与平台定位
抗体偶联药物(ADC)作为肿瘤精准治疗领域的突破性疗法,正经历从"概念验证"到"临床普及"的关键跃迁期。据统计,全球已有超过150款ADC药物进入临床开发阶段,其中十余款产品获批上市,涵盖HER2、TROP2、CD30等多个靶点。然而,ADC药物的开发复杂度远超传统抗体或小分子药物——其结构整合了单克隆抗体、细胞毒性载荷和化学连接子三大组件,涉及靶点选择、偶联工艺、稳定性控制、脱靶毒性预测等多维技术挑战。
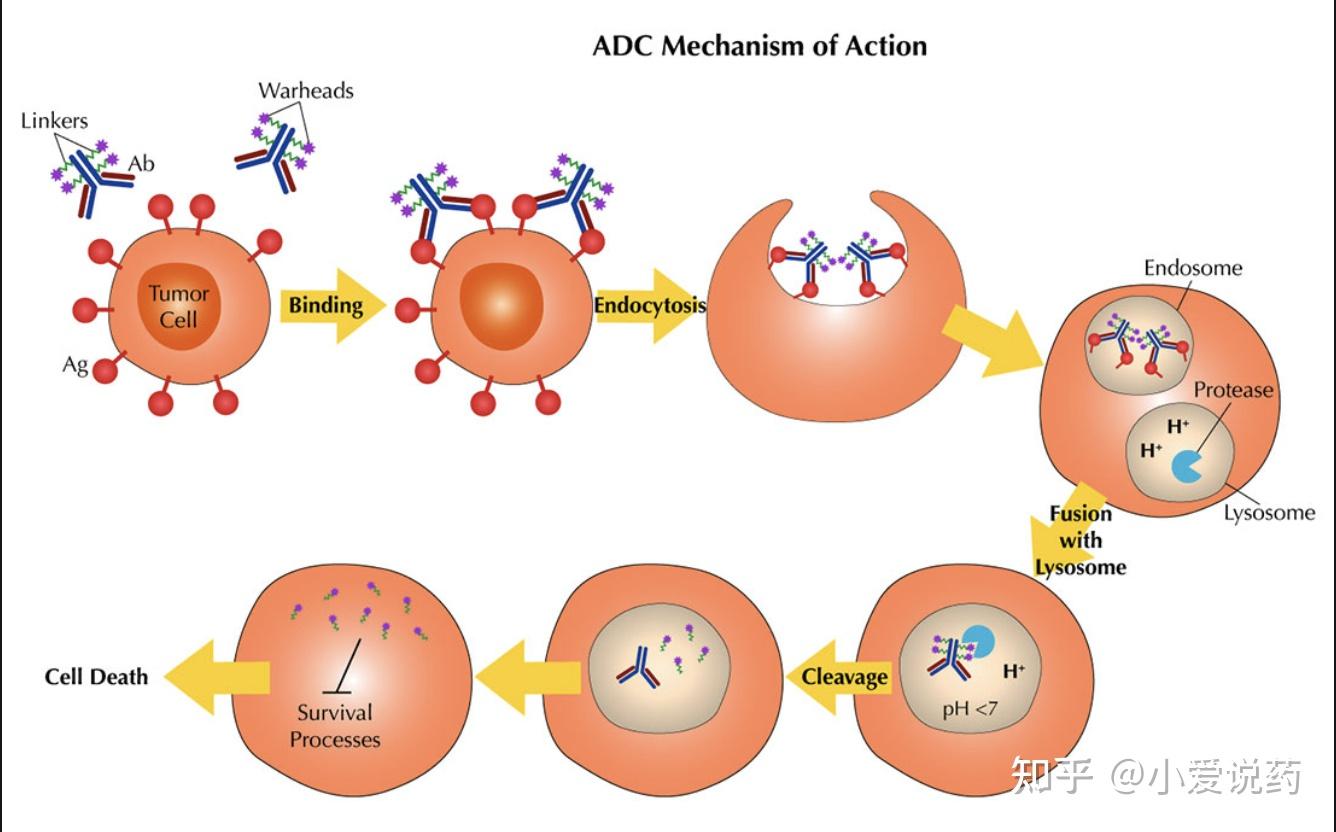
在这一背景下,北京爱思益普生物科技股份有限公司(ICE Bioscience)凭借十余年靶点驱动药物发现的深厚积累,构建了覆盖ADC研发全链条的一体化生物学评价平台。该平台并非简单的技术服务集合,而是以"靶点生物学"为核心竞争力,将分子水平、细胞水平、动物模型及转化科学研究有机整合,形成了独具特色的ADC开发支持体系。
爱思益普的差异化定位体现在两个维度:一是资源储备的广度,平台拥有超过1500个靶点库、900余种细胞系及500余株耐药株、报告基因细胞系;二是技术整合的深度,从早期靶点验证到IND申报,提供模块化与定制化相结合的服务模式。这种"广度+深度"的双轮驱动策略,使其成为全球1000多家新药研发企业的重要合作。
二、核心技术体系解析
2.1 靶点验证与抗体筛选:精准定位的生物学基础
ADC药物的疗效高度依赖靶抗原的选择。理想的ADC靶点需在肿瘤细胞表面高表达、在正常组织低表达,并具备高效的内吞能力。爱思益普的靶点筛选平台建立了超过1200种激酶、200种GPCR受体、100余种离子通道及40多类核受体的筛选体系,为ADC靶点发现提供了丰富的资源库。
在技术手段上,平台采用TR-FRET(时间分辨荧光共振能量转移)和SPR(表面等离子共振)等高精度技术,定量分析抗体与靶抗原的结合亲和力及动力学参数。这些技术不仅能筛选高特异性抗体,还能解析抗体-毒素偶联物的稳定性,为后续优化提供关键数据。值得注意的是,平台针对新兴靶点建立了快速响应机制——例如针对Claudin 18.2这一胃癌热门靶点,迅速开发出基于流式细胞术的靶点表达检测方法,并构建了高表达细胞模型,显著缩短了研发周期。
2.2 偶联工艺优化:稳定性与均一性的技术突破
连接子-载荷系统的设计是ADC研发的核心难点。爱思益普平台深入研究了不同偶联技术的优劣,包括定点偶联(特定氨基酸、非天然氨基酸、酶催化)与随机偶联(链间二硫键、赖氨酸残基)两大路线。在某HER2-ADC项目中,平台通过血浆蛋白酶模拟体系发现传统连接子过早裂解的问题,进而采用PEG化修饰增强亲水性,使药物半衰期从5天延长至12天。
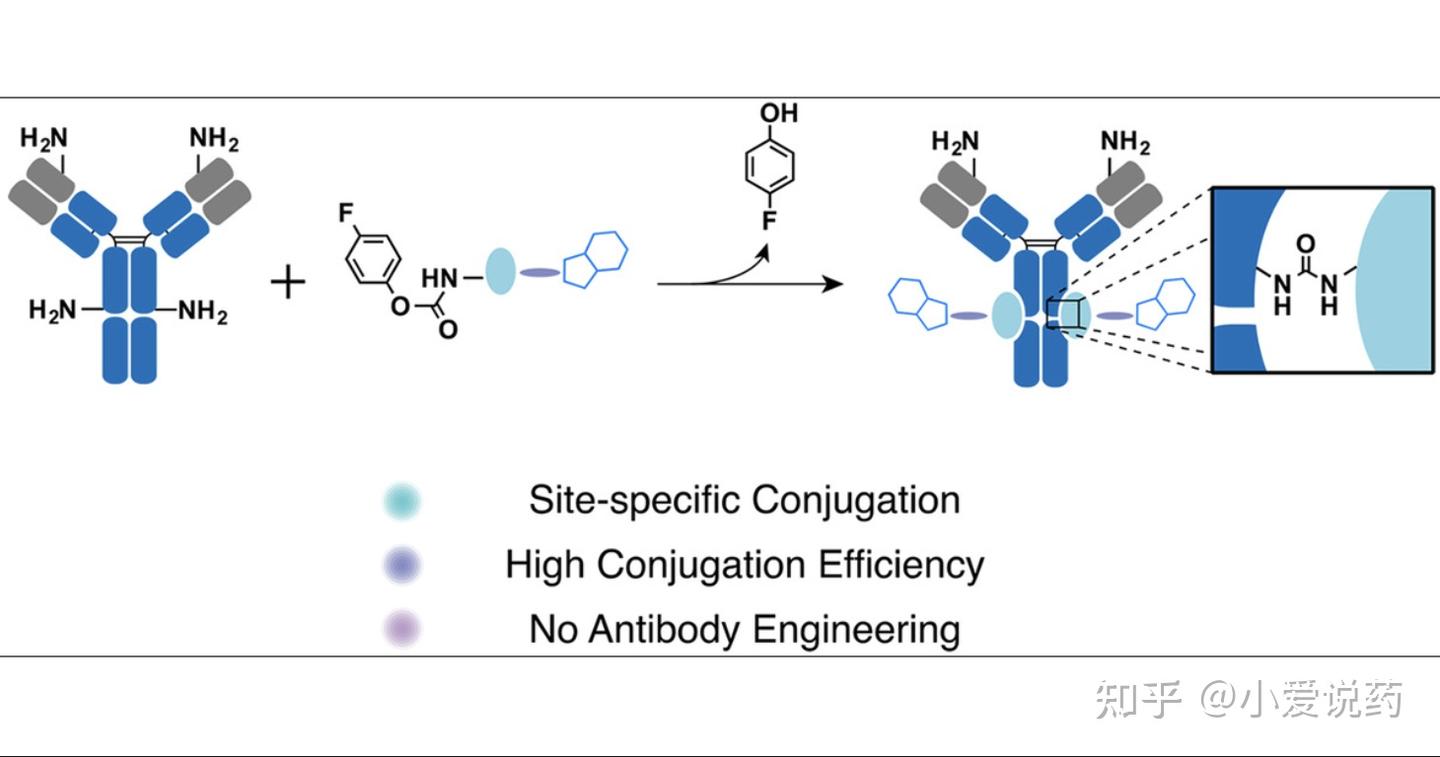
平台还关注DAR(药物抗体比)优化的复杂性。研究表明,高DAR设计虽能提升降解活性,但疏水性可能导致偶联失败或聚集风险[^10^]。通过位点特异性偶联技术,平台提高了ADC分子的均一性,为质量控制和规模化生产奠定了基础。此外,平台整合了FcRn循环机制研究,通过优化抗体Fc段结构减少肾脏清除率,进一步改善药代动力学特征。
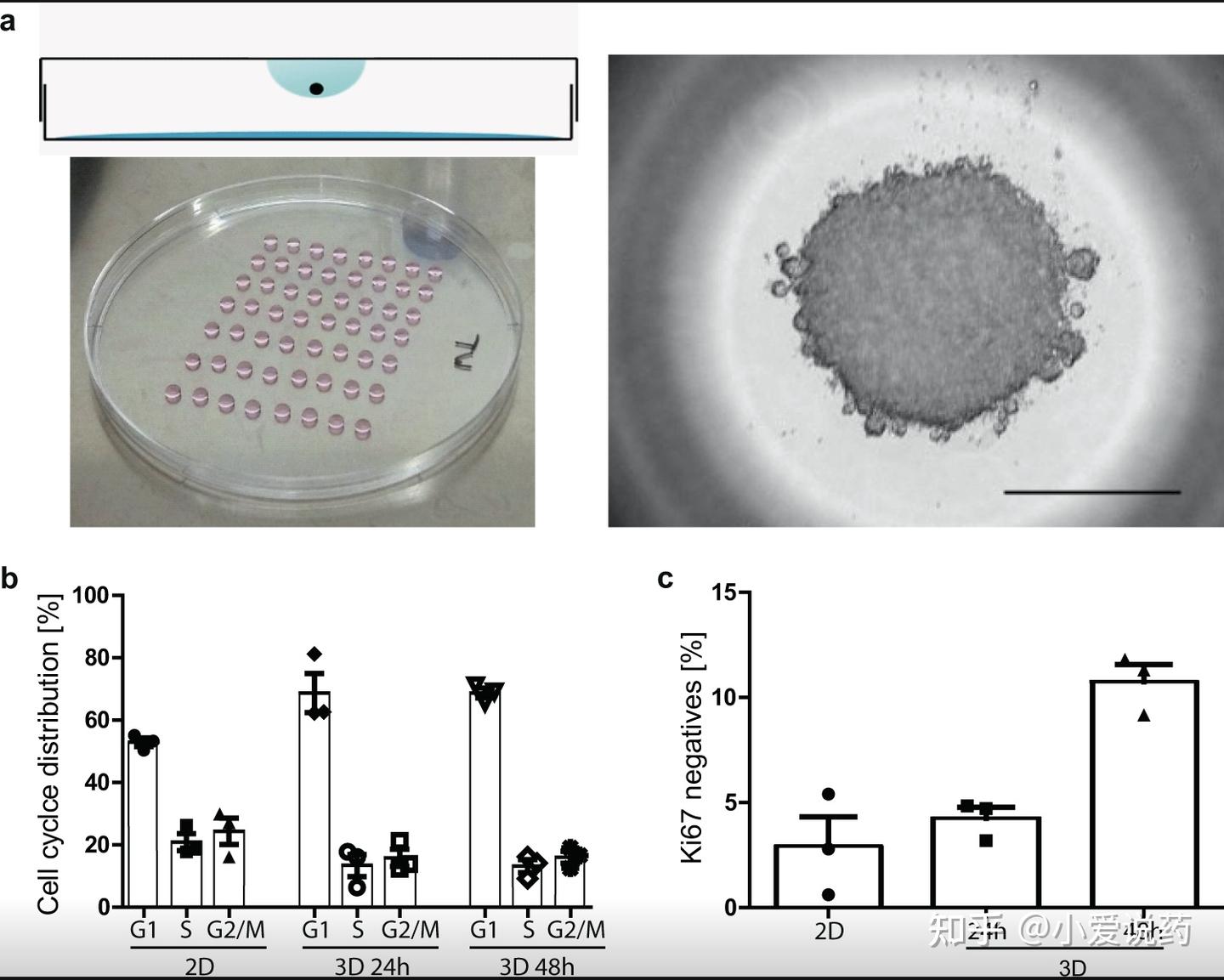
2.3 细胞功能评价:从2D到3D的模型升级
细胞水平药效评价是连接体外研究与体内验证的关键环节。爱思益普建立了涵盖3D增殖、克隆形成、细胞凋亡、细胞周期分析的多维度检测体系。与传统2D培养相比,3D细胞模型能更真实地模拟肿瘤微环境,预测ADC药物的临床疗效。平台拥有900余种细胞系,包括500余种肿瘤细胞系及基因编辑模型,可根据客户需求构建定制化Cell Panel。
在作用机制研究方面,平台不仅关注肿瘤杀伤效果,还深入解析ADC的内吞效率、载荷释放机制及旁观者效应。通过细胞周期分析判断药物是诱导凋亡还是周期阻滞,通过内吞效率检测验证抗体-靶点结合后的内化效果——这些数据为优化毒素载荷与连接子设计提供了重要依据。
2.4 安全性评价:系统性风险管控
ADC药物的脱靶毒性是临床失败的主要原因之一。爱思益普建立了特色的Safety Panel,覆盖90个安全性相关靶点,可系统性预测心血管、神经、代谢、血液等系统的潜在风险。在某TROP2-ADC项目中,平台通过Safety Panel检测发现化合物对肌肉钠通道的潜在抑制作用,经结构优化后治疗窗口提升2.5倍。
平台还整合了hERG通道抑制实验、心肌细胞动作电位检测等心脏安全性评价技术,以及早期ADME/PK研究能力。通过"激酶谱-离子通道-核受体"联合筛选体系,同时评估化合物对多靶点的调控作用,在早期发现潜在毒性问题。此外,平台建立了蛋白质组学脱靶研究能力,通过分析药物与数千种蛋白的相互作用,提前识别毒性风险。
三、一体化服务模式的创新价值
3.1 模块化与定制化的灵活组合
爱思益普的XDC生物学与DMPK一体化评价平台采用"模块化筛选+定制化服务"的混合模式。模块化体系将靶点验证、抗体-毒素偶联优化、细胞功能评价、体内药效验证等环节拆解为标准化单元,客户可根据项目需求灵活组合,显著提高研发效率。例如,在激酶类ADC研发中,平台提供包含500余种激酶靶点的标准化筛选Panel,可同步评估候选分子的活性与选择性。
定制化服务则满足差异化需求。平台支持全流程定制化研发,可根据客户项目特点设计专属技术方案。在某罕见病ADC研发中,平台通过基因编辑技术构建特定突变型细胞系,模拟患者肿瘤微环境,最终开发出针对该罕见病的高效ADC分子。这种灵活性在个性化医疗时代尤为重要。
3.2 DMPK与生物分析的深度整合
ADC药物的PK/PD研究具有独特复杂性——需同时监测完整ADC、总抗体、游离载荷及代谢产物等多种分析物。爱思益普平台整合了DMPK筛选、早期ADME研究及定制化动物模型开发能力,通过自动化组织匀浆系统与LC-MS/MS技术,实现96孔板规格样本的快速处理,单次实验同步获取药物在血浆、脑、肝、肾等组织中的浓度数据。
平台还建立了免疫原性(ADA)评价能力,监测抗药抗体对有效性和安全性的影响。对于新型载荷,平台开展体外ADME研究(尤其是外排转运体检测)、体内代谢产物鉴定(Met ID)等深入研究,为临床剂量选择和风险管控提供数据支撑。
3.3 转化科学研究:从实验室到临床的桥梁
爱思益普强调转化科学在ADC开发中的价值。平台通过建立类器官与患者来源肿瘤异种移植(PDX)模型,提升ADC药物的精准度与临床转化率。在体内药效验证中,平台不仅关注肿瘤抑制率(TGI),还深入分析载荷在肿瘤组织与非靶组织的分布差异,解释疗效与安全性的平衡机制。
这种转化导向的研究模式已产生实际成果。目前,平台已支持全球药企完成数十项ADC项目的IND申报,其中多款针对HER2、TROP2等靶点的创新药物正在开展Ⅱ期或Ⅲ期临床试验。这些数据证明了平台在推动ADC药物从实验室到临床转化方面的卓越能力。
四、前沿技术布局与未来展望
4.1 新型载荷与连接子的探索
随着ADC技术迭代,新型载荷如DNA损伤修复抑制剂(DDRi)、靶蛋白降解剂(PROTAC)、免疫激动剂等逐渐进入研发视野。爱思益普平台已建立特色的双载荷或多载荷Cell Panel筛选解决方案,支持新型payload的活性评价。在PROTAC-ADC(DAC)领域,平台通过案例研究展示了不同设计策略的优劣——例如GNE-987通过二硫键连接子与CLL1抗体偶联,在AML小鼠模型中表现出显著疗效;而HER2抗体通过硫醇再桥接技术偶联VHL基PROTAC,利用溶酶体酯酶切割实现靶蛋白降解。
4.2 AI驱动的药物发现
近年来,爱思益普在AI驱动药物发现领域取得积极进展。通过整合机器学习算法与高通量筛选数据,平台可预测ADC分子的成药性、优化DAR值设计、加速先导化合物筛选。这种"AI+生物学"的融合模式,有望进一步提升ADC研发效率,降低试错成本。

4.3 国际化服务能力建设
2024年5月,爱思益普完成B++轮融资,由亦庄国投领投,雅惠投资继续增持。本轮融资将支持公司为海内外制药公司提供更领先、更优质的服务。目前,平台已建立符合国际标准的药物发现与早期筛选体系,支持全球客户的IND申报需求。

扫一扫关注
爱思益普公众号


业务咨询
北京
业务咨询专线:010-6780-9840
联系地址:北京市经济技术开发区科创十三街18号院锋创科技园16号楼
上海
业务咨询专线:010-6780-9840
联系地址:上海市浦东新区蔡伦路780号新技术推广大楼3E5O室
徐州
业务咨询专线:010-6780-9840
联系地址:江苏省徐州市云龙区淮海文博园 二号楼2层
贵州
业务咨询专线:010-6780-9840
联系地址:贵州省贵阳市南明区龙岭路50号 欧美医药产业园一期2号楼



