
领跑靶点驱动药物发现一体化服务的爱思益普科研团队精心打造了一款针对耐受PARP抑制剂后药物筛选或优化治疗方式的评价系统,可满足后续新型药物或者联合用药等药物或者治疗方式研究的一体化服务平台。


聚ADP核糖聚合酶 (Poly ADP-ribose Polymerase ,PARP)通过对蛋白的聚ADP核糖基化进而参与蛋白翻译后修饰,进而帮助细胞对损伤的DNA进行修复。其杀伤肿瘤细胞的机制是利用肿瘤细胞自身存在的DNA修复缺陷基因(例如BRCA基因突变),在通过抑制PARP酶阻断另外一条DNA修复通路,从而导致癌症细胞死亡。
PARP抑制剂(PARPi)是第一种成功利用合成致死 (Synthetic Lethality) 概念获得批准在临床使用的抗癌药物,其具有显著的疗效。截止目前为止,全球已有7款PARP抑制剂上市(Olaparib、Rucaparib、Talazoparib、Fluzoparib、Pamiparib和Senaparib),中国也有5款药物上市,主要适应为内分泌有关的肿瘤,例如卵巢癌、乳腺癌、前列腺癌和胰腺癌。虽然疗效显著,但耐药问题一直是困扰临床的主要问题,卵巢癌平均无进展期约21个月,其他癌种则在6-12月内就会出现耐受。耐受后的治疗如何治疗将是医生、患者和药物研发者特别关注的问题。
爱思益普体内药理团队,已经构建A2780/Olaparib-R、A2780/Olaparib-R、HCC1806/Niraparib-R、HCC1806/Talazoparib-R、MDA-MB-468/Olaparib-R和PANC-1/Talazoparib-R耐药株。其中已经对以下5株耐药株完成体内建模。
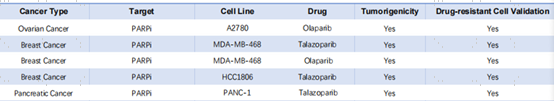
案例分享:
耐受奥拉帕利的乳腺癌模型
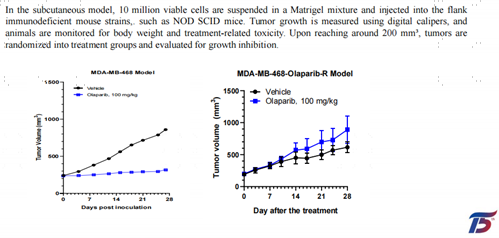
此外,爱思益普体内药理平台还建立了多种特色平台:
EGFR抑制剂相关体内耐药模型
KRAS/BRAF相关体内耐药模型
ALK融合突变相关体内耐药模型
结直肠肿瘤体内耐药模型
AR+前列腺癌耐药模型
ADC及Payload耐药模型
自免和炎症药理平台



