临床主要表现:核心认知域损害需至少包括记忆障碍、执行功能障碍、语言障碍、视空间能力障碍中的一项。伴随症状常见精神行为异常,如淡漠、抑郁、焦虑、激越、幻觉及睡眠紊乱等,约80%患者病程中会出现。
核心机制:Aβ沉积形成淀粉样斑块,Tau蛋白过度磷酸化形成神经元纤维缠结(NFTs)
l 模型种类齐全:覆盖化学诱导(STZ、Aβ1-42、东莨菪碱)与转基因(APP/PS1)模型
l 体外体内联动:从原代神经元机制到行为验证的全链条服务
l 多维度评价体系:行为学+分子病理+免疫荧光,全面评估药效
l 实验流程标准化:严格遵循国际protocols,数据可靠
l 灵活服务模式:支持单模型测试、药物筛选、机制研究、阳性药验证
l 病理机制覆盖全面:涵盖Aβ沉积、Tau磷酸化、神经炎症、胆碱能损伤等多靶点
l 模型周期可选:急性模型(东莨菪碱、Aβ注射)适合快速筛选,慢性模型(STZ、APP/PS1)适合机制研究和长期药效评价
l 旷场测试(OFT):评估自主活动与焦虑样行为
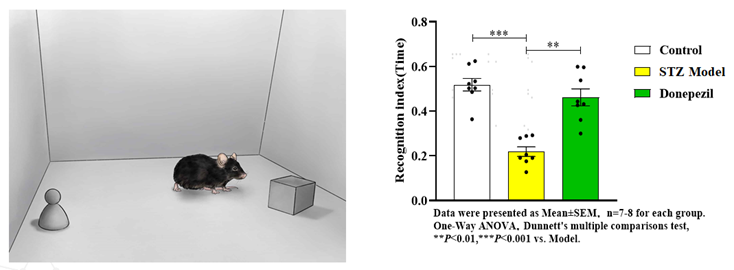
l 新物体识别测试(NOR):评估识别记忆
l Y迷宫测试:评估工作记忆
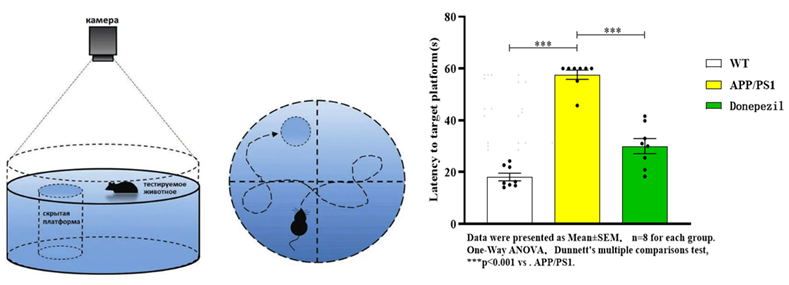
l 水迷宫测试(MWM):评估空间学习与记忆能力
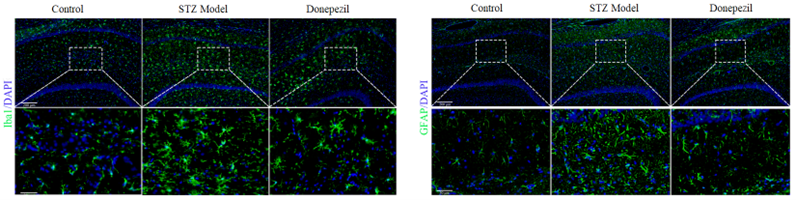
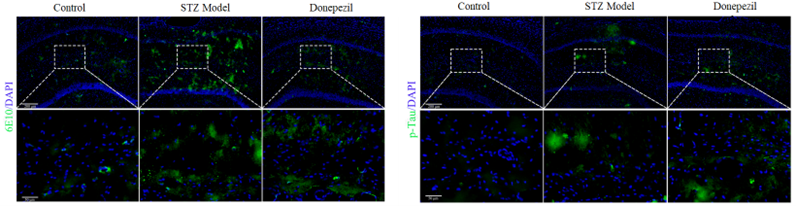
l 免疫荧光染色:Aβ沉积(6E10)、Tau/p-Tau等
l Elisa检测:炎症因子(TNF-α、IL-6、IL-1β)等
l 细胞活力检测:CCK-8、LDH释放
l 神经元形态分析:突触可塑性、神经突生长
|
模型类型 |
造模方式 |
检测指标 |
|
SH-SY5Y/原代海马神经元细胞模型 |
Glutamic acid / OA / Aβ1-42/H2O2 |
CCK-8、LDH释放、免疫荧光(Tau/p-Tau)、神经元形态分析 |
l 多指标联合检测(细胞活力、细胞毒性、Tau蛋白磷酸化)
l 支持药物筛选、机制研究、阳性药验证
l 原代神经元更接近体内生理状态
l 可定制化造模方案(浓度梯度、时间梯度)
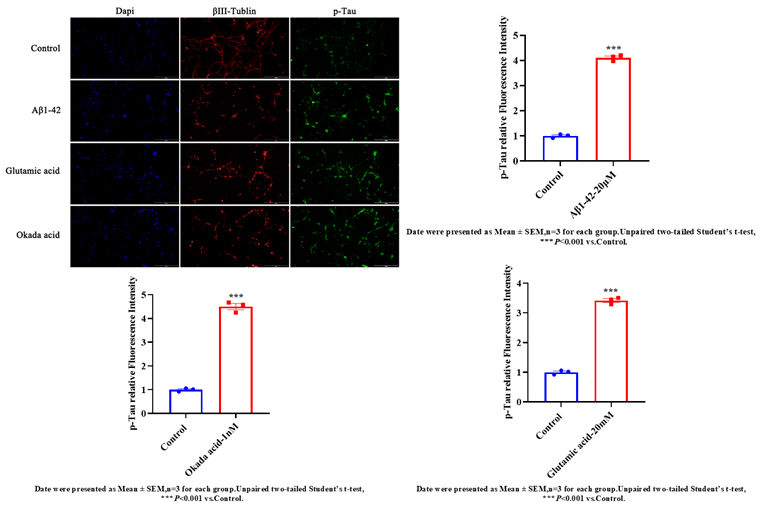
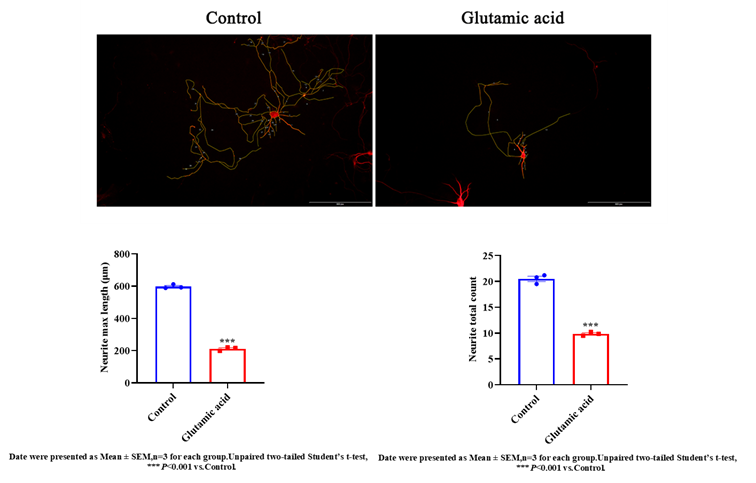
我们建立并优化了多种国际公认的AD动物模型,涵盖化学诱导、转基因等多种类型,满足不同研究需求。
|
模型类型 |
模型方法 |
核心机制 |
检测指标 |
|
STZ诱导大鼠AD模型 |
双侧侧脑室注射STZ |
脑内胰岛素信号受损,葡萄糖代谢减退 |
OFT、NOR、Y迷宫、MWM、Elisa(TNF-α、IL-6、IL-1β)、免疫荧光(6E10、p-Tau) |
|
Aβ1-42诱导小鼠AD模型 |
双侧海马注射Aβ1-42寡聚体 |
Aβ直接神经毒性,神经炎症 |
|
|
东莨菪碱诱导大鼠AD模型 |
腹腔注射东莨菪碱 |
阻断胆碱能投射,AChE活性升高,ACh水平降低 |
|
|
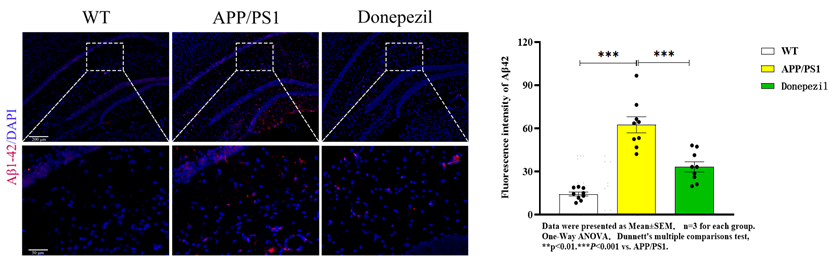
APP/PS1转基因小鼠模型 |
转染人突变APP和PS1基因 |
Aβ沉积加速,神经炎性斑形成 |
l 模型种类全面:涵盖化学诱导(STZ、Aβ1-42、东莨菪碱)与转基因(APP/PS1)模型,满足不同机制研究需求
l 行为学评价体系完善:旷场、新物体识别、Y迷宫、水迷宫等多维度评估认知功能
l 病理检测全面:6E10染色评估Aβ沉积,p-Tau检测Tau蛋白磷酸化,Elisa检测神经炎症因子
l 疾病进展模拟:STZ模型模拟散发性AD的胰岛素信号受损,Aβ注射模型模拟Aβ直接神经毒性,APP/PS1模型模拟家族性AD的渐进性病理改变
l 多物种选择:小鼠、大鼠模型均可提供
l 给药方案灵活:支持单次给药、重复给药、预防性给药等多种研究设计