News Detail
 来源:2026-04-20 13:16:59
来源:2026-04-20 13:16:59
 浏览量:16624
浏览量:16624
引言:ADC 药物研发的复杂性与服务需求
抗体偶联药物(Antibody-Drug Conjugate, ADC)作为肿瘤精准治疗领域的突破性疗法,正经历从「概念」证「到「临床」的关键跃迁期。据统计,全球已有超过 150 款 ADC 药物进入临床开发阶段,其中十余款产品获批上市,涵盖 HER2、TROP2、CD30 等多个靶点。然而,ADC 药物的开发复杂度远超传统抗体或小分子药物——其结构整合了单克隆抗体、细胞毒性载荷和化学连接子三大组件,涉及靶点选择、偶联工艺、稳定性控制、脱靶毒性预测等多维技术挑战。
在这一背景下,专业化合同研究组织(CRO)的服务能力成为创新药企突破技术瓶颈的关键支撑。北京爱思益普生物科技股份有限公司凭借十余年靶点驱动药物发现的深厚积累,构建了覆盖 ADC 研发全链条的一体化生物学评价平台。该平台并非简单的技术服务集合,而是以「靶点生物学」为核心竞争力,将分子水平、细胞水平、动物模型及转化科学研究有机整合,形成了独具特色的 ADC 开发支持体系。
爱思益普的差异化定位体现在两个维度:
📚 一是资源储备的广度,平台拥有超过 1500 个靶点库、900 余种细胞系及 500 余株耐药株、报告基因细胞系;
📚 二是技术整合的深度,从早期靶点验证到 IND 申报,提供模块化与定制化相结合的服务模式。这种「广度+深度」的双轮驱动策略,使其成为全球 1000 多家新药研发企业的重要合作伙伴。
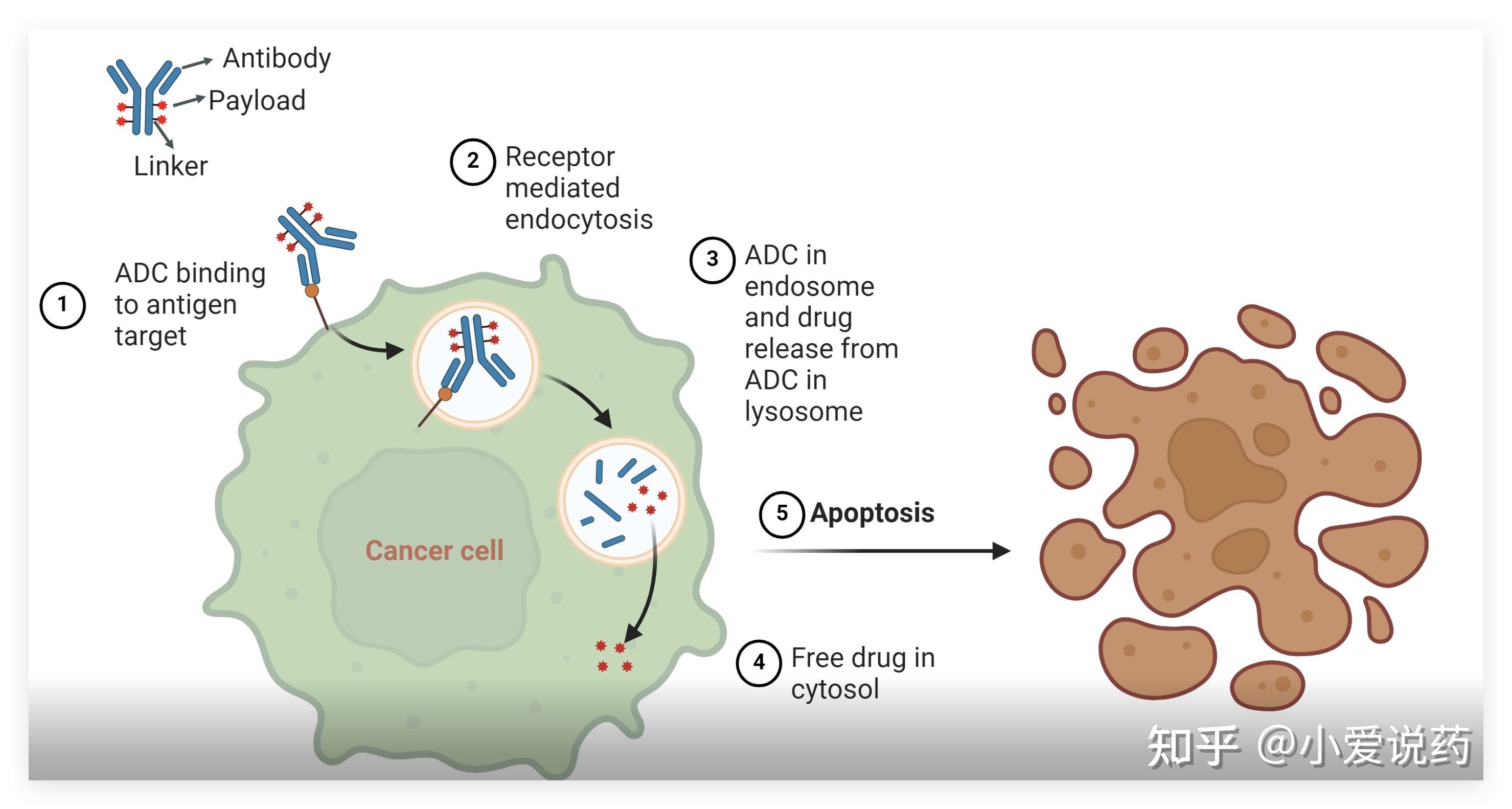
一、靶点验证与抗体筛选:精准定位的生物学基础
1.1 靶点选择的科学逻辑
ADC 药物的疗效高度依赖靶抗原的选择。理想的 ADC 靶点需在肿瘤细胞表面高表达、在正常组织低表达,并具备高效的内吞能力。爱思益普的靶点筛选平台建立了超过 1200 种激酶、200 种 GPCR 受体、100 余种离子通道及 40 多类核受体的筛选体系,为 ADC 靶点发现提供了丰富的资源库。
在技术手段上,平台采用 TR-FRET(时间分辨荧光共振能量转移)和 SPR(表面等离子共振)等高精度技术,定量分析抗体与靶抗原的结合亲和力及动力学参数。这些技术不仅能筛选高特异性抗体,还能解析抗体-毒素偶联物的稳定性,为后续优化提供关键数据。值得注意的是,平台针对新兴靶点建立了快速响应机制——例如针对 Claudin 18.2 这一胃癌热门靶点,迅速开发出基于流式细胞术的靶点表达检测方法,并构建了高表达细胞模型,显著缩短了研发周期。
1.2 抗体发现与功能表征
抗体是 ADC 药物的「导航系统」,其亲和力和特异性直接决定药物的靶向能力和治疗窗口。爱思益普建立了完善的抗体发现与表征平台,包括杂交瘤技术、噬菌体展示、单 B 细胞克隆等多种抗体发现策略。通过表面等离子共振(SPR)技术,可精确测定抗体与靶抗原的结合动力学参数,包括结合速率常数(ka)、解离速率常数(kd)和平衡解离常数(KD)。
在 ADC 药物开发中,抗体内化效率是影响药效的关键因素。爱思益普开发了基于流式细胞术和共聚焦显微镜的抗体内化检测方法,可定量评估抗体-受体复合物进入细胞的效率和动力学。此外,平台还提供抗体 Fc 功能检测,包括抗体依赖性细胞介导的细胞毒性(ADCC)、补体依赖性细胞毒性(CDC)和抗体依赖性细胞吞噬(ADCP),全面评价抗体的效应功能。”
二、连接子-载荷偶联技术:稳定性与均一性的工程突破
2.1 偶联工艺的技术路线
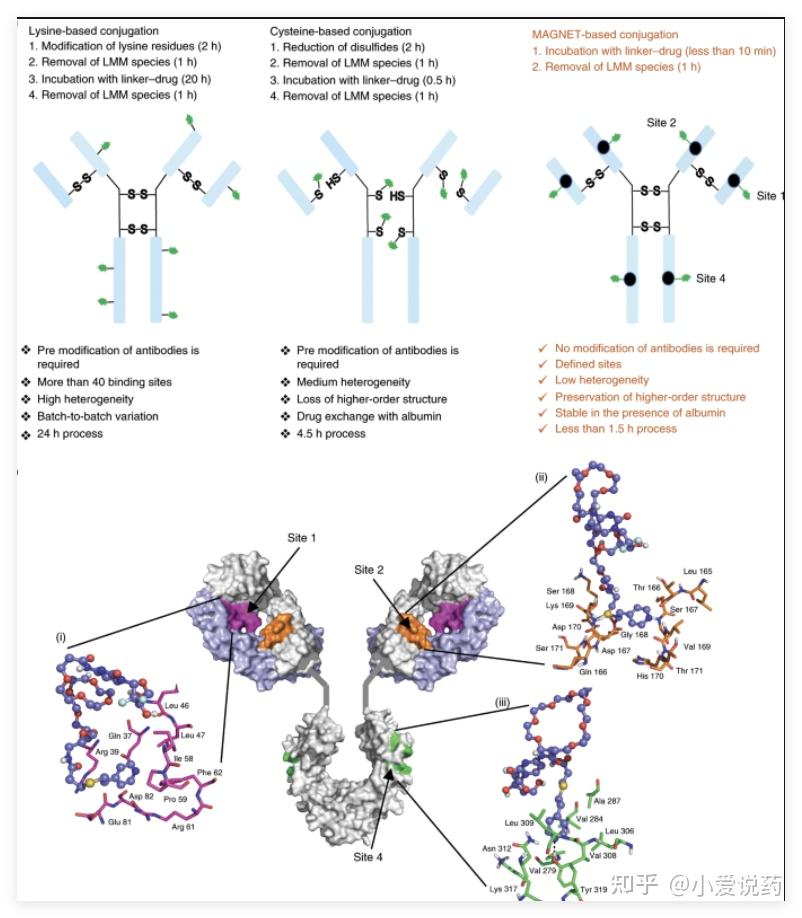
连接子是 ADC 药物的「桥梁」,其设计需要在循环稳定性和肿瘤释放效率之间取得平衡。爱思益普提供多种偶联化学策略,包括赖氨酸侧链偶联、半胱氨酸桥连偶联以及定点偶联技术。通过质谱分析和疏水相互作用色谱(HIC),可精确表征 ADC 的 DAR(药物抗体比)分布和偶联位点。
定点偶联技术是新一代 ADC 开发的重要方向。与传统随机偶联相比,定点偶联可实现均一的 DAR 值和确定的偶联位点,提高药物的药代动力学性质和稳定性。爱思益普的定点偶联平台支持多种技术路线,包括工程化半胱氨酸、非天然氨基酸插入、酶催化偶联等,满足不同 ADC 项目的需求。”
2.2 连接子稳定性优化
平台深入研究了不同偶联技术的优劣,包括定点偶联(特定氨基酸、非天然氨基酸、酶催化)与随机偶联(链间二硫键、赖氨酸残基)两大路线。在某 HER2-ADC 项目中,平台通过血浆蛋白酶模拟体系发现传统连接子过早裂解的问题,进而采用 PEG 化修饰增强亲水性,使药物半衰期从 5 天延长至 12 天。
平台还深入研究 FcRn 循环机制,通过优化抗体的 Fc 段结构,减少肾脏清除率,进一步提升药物在血液循环中的稳定性。这种多维度优化策略,使 ADC 分子在保持肿瘤靶向性的同时,显著改善了药代动力特征。
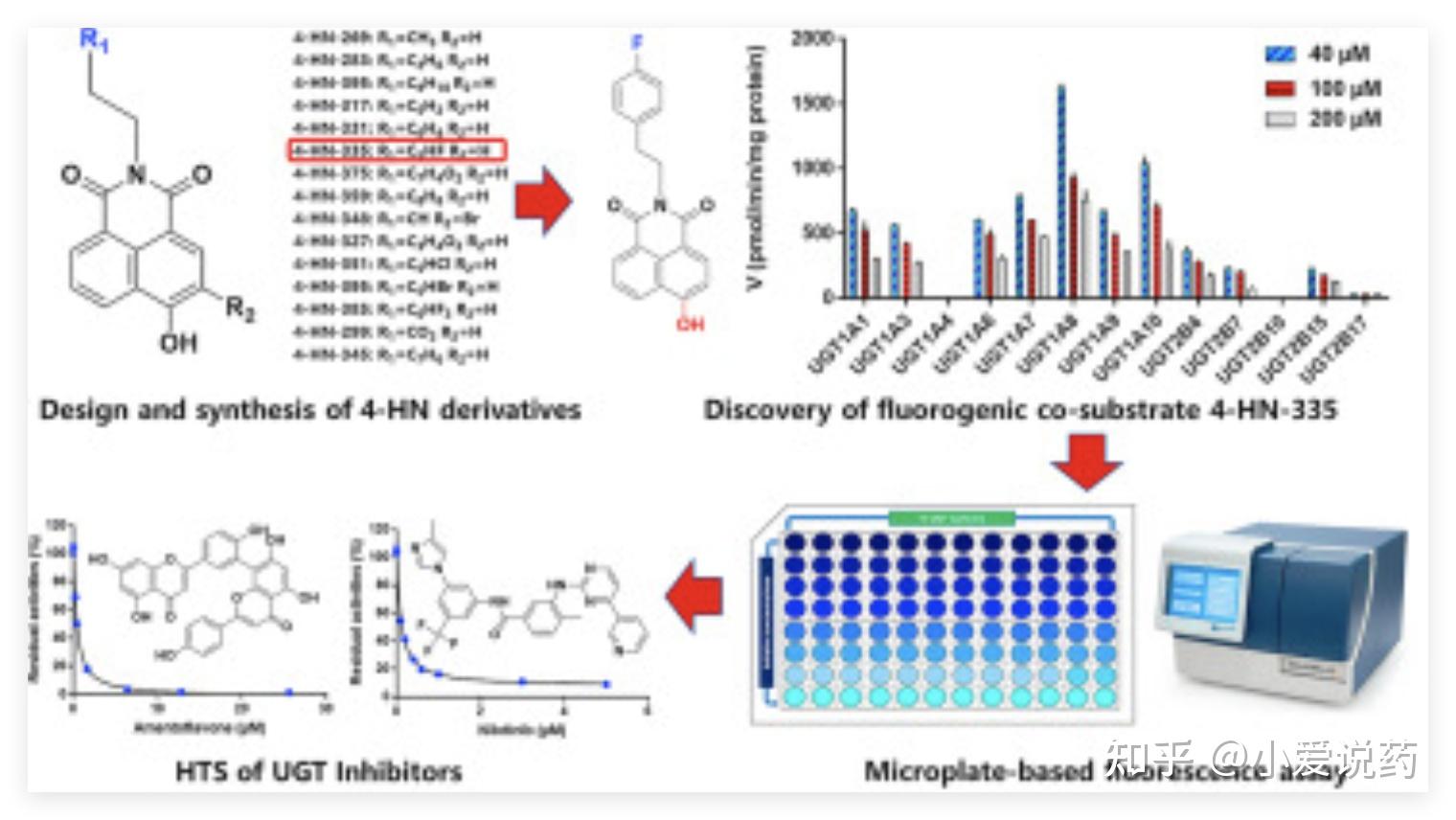
三、体外药效评价:从分子机制到细胞功能的多维验证
3.1 细胞水平的功能验证
ADC 药物的体外药效评价需要模拟体内作用机制,包括靶点结合、内吞、溶酶体降解和药物释放等多个环节。爱思益普建立了基于靶抗原阳性细胞系的 ADC 细胞杀伤实验,通过 CellTiter-Glo 或 CCK-8 方法测定半数抑制浓度(IC50),评价 ADC 的选择性杀伤活性。
针对 ADC 的特殊作用机制,平台还开发了特异性检测方法。通过 pH 敏感染料标记,可实时监测 ADC 的内吞和溶酶体转运过程。利用溶酶体抑制剂(如氯喹、巴弗洛霉素 A1)处理,可验证 ADC 的溶酶体依赖性杀伤机制。此外,平台还提供旁观者效应(Bystander Effect)检测,评估释放的载荷对邻近抗原阴性肿瘤细胞的杀伤能力,这对治疗异质性肿瘤具有重要意义。”
3.2 定制化 Cell Panel 筛选
平台的特色服务体现在定制化 Cell Panel 的应用上。在某 HER2-ADC 项目中,平台利用定制化 Cell Panel 服务,发现特定细胞系对 ADC 的敏感性差异,指导优化毒素载荷与连接子设计。这种从靶点到药效的闭环验证体系,显著提升了研发效率。
平台拥有 900 余种细胞库,包含 500 余种肿瘤细胞系及基因编辑模型。通过 3D 增殖、克隆形成等多样化检测手段,平台可评估 ADC 分子对肿瘤细胞的杀伤效果。这种资源组合为 ADC 研发提供了多样化的实验基础,能够满足不同疾病领域靶点筛选的需求。
四、生物分析与 DMPK 研究:药代动力学的精准解析
4.1 DAR 值测定与质量控制
药物抗体比(DAR)是 ADC 药物的关键质量属性,影响药效、安全性和药代动力学。
爱思益普提供多种 DAR 测定方法:
⏰️ 疏水相互作用色谱(HIC):根据 DAR 值不同导致的疏水性差异,分离不同偶联形式的 ADC,通过紫外检测器定量各组分的相对丰度。该方法保持 ADC 的完整性,适用于过程控制和稳定性研究。
⏰️ 还原质谱法:通过还原二硫键将 ADC 分解为轻链和重链,利用高分辨质谱测定各组分的分子量,计算平均 DAR 值和 DAR 分布。该方法分辨率高,可精确识别不同偶联位点。
⏰️ 酶解质谱法:使用 IdeS 蛋白酶或还原剂处理 ADC,结合液相色谱-质谱联用(LC-MS)分析,获得详细的 DAR 分布和偶联位点信息。该方法信息丰富,适用于深度表征。
4.2 药代动力学与免疫原性分析
ADC 药物的 PK 特征复杂,总抗体、偶联抗体和游离载荷具有不同的消除动力学。爱思益普建立了基于 ELISA 和电化学发光(ECL)的免疫分析方法,分别检测总抗体(不区分是否偶联载荷)和偶联抗体(仅检测携带载荷的抗体)。通过两种检测方法的差异,可间接反映 ADC 在体内的载荷释放情况。
对于载荷和连接子-载荷代谢物,平台开发了高灵敏度的 LC-MS/MS 方法,支持多种生物基质(血浆、血清、组织)的定量分析。考虑到载荷的高活性,方法验证特别关注灵敏度、选择性和稳定性,确保数据的准确性和可靠性。
在免疫原性评价方面,平台建立了多层级免疫原性检测策略,包括筛选、确证和中和抗体检测。针对 ADC 的特殊性,平台可分别检测针对抗体部分、连接子-载荷部分的免疫反应,帮助理解免疫原性的来源和临床意义“。
五、安全性评价:系统性风险管控与脱靶毒性预测
5.1 Safety Panel 脱靶筛选
ADC 药物的脱靶毒性是临床失败的主要原因之一。爱思益普建立了特色的 Safety Panel,覆盖 90 个安全性相关靶点,可系统性预测心血管、神经、代谢、血液等系统的潜在风险。在某 TROP2-ADC 项目中,平台通过 Safety Panel 检测发现化合物对肌肉钠通道的潜在抑制作用,经结构优化后治疗窗口提升 2.5 倍。
平台还整合了 hERG 通道抑制实验、心肌细胞动作电位检测等心脏安全性评价技术,以及早期 ADME/PK 研究能力。通过「激酶谱-离子通道-核受体」联合筛选体系,同时评估化合物对多靶点的调控作用,在早期发现潜在毒性问题。此外,平台建立了蛋白质组学脱靶研究能力,通过分析药物与数千种蛋白的相互作用,提前识别毒性风险。
5.2 组织交叉反应研究
ADC 药物的安全性评价需要关注抗体相关毒性和载荷相关毒性。爱思益普提供基于细胞的脱靶筛选(Safety Panel),检测 ADC 对正常组织的交叉反应。通过组织交叉反应(TCR)研究,可识别 ADC 与正常组织的非特异性结合,预测临床毒性风险。
在某 TROP2-ADC 研发中,平台通过 Safety Panel 检测发现化合物对心脏钾通道的潜在抑制风险,经结构优化后成功消除心脏毒性,为药物进入临床提供安全保障。这种系统性的安全性评价平台,为 ADC 研发提供了从早期筛选到临床前验证的全流程安全保障。
六、体内药效验证:从体外到临床的转化桥梁
6.1 动物模型与药效评价
平台建立了多种肿瘤异种移植模型(CDX)和患者来源异种移植模型(PDX),支持 ADC 的体内药效评价。通过生物发光成像(BLI)或磁共振成像(MRI),可实时监测肿瘤生长和治疗响应。针对 ADC 的特殊毒性,平台还提供脱靶毒性评估,包括皮肤毒性、眼毒性和神经毒性检测。
在某 TROP-2-ADC 项目中,平台通过体内药效模型发现候选分子在乳腺癌异种移植模型中的肿瘤抑制率达 85%,同时通过心脏安全性评价排除 hERG 通道抑制风险,为药物进入临床阶段提供双重保障。
6.2 DMPK 与早期 ADME 研究
平台整合了 DMPK 筛选、早期 ADME 研究及定制化动物模型开发能力。通过自动化组织匀浆系统与 LC-MS/MS 技术,平台可实现 96 孔板规格样本的快速处理,单次实验同步获取药物在血浆、脑、肝、肾等组织中的浓度数据,为药代动力学研究提供高效支持。
平台还通过定制化动物模型开发,模拟特定疾病状态下的药物响应。例如,在某 PD-L1-ADC 项目中,平台通过构建人源化肿瘤移植模型,发现候选分子在免疫检查点抑制剂耐药肿瘤中的协同杀伤作用,指导优化联合用药策略。这种从体外到体内的闭环验证体系,使爱思益普的 ADC 平台成为全球药企研发的首选合作伙伴。
七、新一代 ADC 技术平台:前沿布局与创新探索
7.1 双特异性 ADC 与双药 ADC
随着 ADC 技术迭代,新型 ADC 形式不断涌现。爱思益普紧跟技术前沿,建立了支持新一代 ADC 开发的服务能力。双特异性抗体可同时识别两个不同靶点,提高肿瘤选择性和内化效率。爱思益普支持双特异性 ADC 的开发,包括靶点组合筛选、双抗构建和偶联优化。
双药 ADC 在同一抗体上偶联两种不同作用机制的载荷,可同时攻击肿瘤细胞的多个信号通路,降低耐药风险。爱思益普建立了双药偶联工艺和分析方法,支持不同载荷组合的筛选和优化。通过精确控制两种载荷的比例和 DAR 值,实现协同增效。
7.2 免疫刺激型 ADC(ISAC)
免疫刺激型 ADC(ISAC)将细胞毒载荷替换为免疫激动剂(如 TLR 激动剂、STING 激动剂),在靶向递送的同时激活肿瘤免疫微环境。爱思益普提供 ISAC 的筛选和评价服务,包括免疫激活检测、细胞因子释放分析和体内药效评价,助力肿瘤免疫联合治疗策略的开发。
7.3 AI 驱动的药物发现
近年来,爱思益普在 AI 驱动药物发现领域取得积极进展。通过整合机器学习算法与高通量筛选数据,平台可预测 ADC 分子的成药性、优化 DAR 值设计、加速先导化合物筛选。这种「AI+生物学」的融合模式,有望进一步提升 ADC 研发效率,降低试错成本。
在新型载荷探索方面,平台已建立特色的双载荷或多载荷 Cell Panel 筛选解决方案,支持新型 payload 的活性评价。在 PROTAC-ADC(DAC)领域,平台通过案例研究展示了不同设计策略的优劣。
八、服务模式与质量保障:灵活高效的协作体系
8.1 模块化与定制化的灵活组合
爱思益普的 XDC 生物学与 DMPK 一体化评价平台采用「模块化筛选+定制化服务」的混合模式。模块化体系将靶点验证、抗体-毒素偶联优化、细胞功能评价、体内药效验证等环节拆解为标准化单元,客户可根据项目需求灵活组合,显著提高研发效率。
例如,在激酶类 ADC 研发中,平台提供包含 500 余种激酶靶点的标准化筛选 Panel,可同步评估候选分子的活性与选择性。这种转化导向的研究模式已产生实际成果——目前,平台已支持全球药企完成数十项 ADC 项目的 IND 申报,其中多款针对 HER2、TROP2 等靶点的创新药物正在开展Ⅱ期或Ⅲ期临床试验。
8.2 质量保障与国际化布局
爱思益普 ADC 药物筛选服务平台具有以下核心优势:
🔑 技术整合能力:从抗体发现、偶联工艺到生物分析,提供一站式技术解决方案,减少项目交接成本和时间损耗。
🔑 质量保障体系:建立完善的质量管理体系,符合 GLP 规范要求,数据可用于 IND 申报和临床申请。
🔑 灵活合作模式:支持项目制合作(Fee-for-Service)和战略合作(Strategic Partnership),根据客户需求定制服务方案。
🔑 快速响应机制:专业的项目管理团队,确保实验进度和数据交付的及时性,加速客户研发进程。
2024 年 5 月,爱思益普完成 B++轮融资,由亦庄国投领投,雅惠投资继续增持。本轮融资将支持公司为海内外制药公司提供更领先、更优质的服务。目前,平台已建立符合国际标准的药物发现与早期筛选体系,支持全球客户的 IND 申报需求。
结语:构建 ADC 研发的中国方案
ADC 药物作为肿瘤精准治疗的重要方向,正处于快速发展期。爱思益普依托大分子分析部的技术平台,构建了覆盖 ADC 研发全链条的筛选服务体系,助力创新药企突破技术瓶颈,加速新药上市进程。
从靶点验证的精准定位,到偶联工艺的技术突破;从体外药效的多维评价,到体内转化的闭环验证;从传统细胞毒 ADC,到双特异性、免疫刺激型等新一代技术——爱思益普以「靶点生物学」为核心,形成了独具特色的 ADC 开发支持体系。随着双特异性 ADC、双药 ADC 等新一代技术的成熟,ADC 药物将在肿瘤治疗中发挥更加重要的作用。
爱思益普将持续投入技术创新,与合作伙伴共同推动 ADC 药物研发进入新纪元,为全球患者提供更多、更好的治疗选择!