News Detail
 来源:2026-04-02 09:20:48
来源:2026-04-02 09:20:48
 浏览量:12174
浏览量:12174
一、CDX 模型的技术定位与核心价值
CDX(Cell Line-Derived Xenograft,细胞系来源异种移植)模型是抗肿瘤药物临床前研究中使用最广泛的体内评价平台。该模型通过将体外培养的人源肿瘤细胞系移植至免疫缺陷小鼠体内,建立可稳定传代的实体瘤体系,为新药筛选提供标准化、可重复的体内数据。
相较于 PDX(人源肿瘤组织移植)模型,CDX 模型具有成瘤周期短(7-14 天)、批次一致性高(CV<20%)、成本可控等显著优势,特别适用于早期药物筛选、机制研究和 IND 申报阶段的药效概念验证。据统计,全球约 70% 的抗肿瘤药物临床前研究依赖 CDX 模型完成初步体内评价。
爱思益普建立的 CDX 模型构建服务体系,覆盖模型设计、细胞制备、动物接种、质量验证、药效评价五大模块,形成从体外到体内的完整技术闭环,为制药企业提供符合国际申报标准的临床前研究支持。
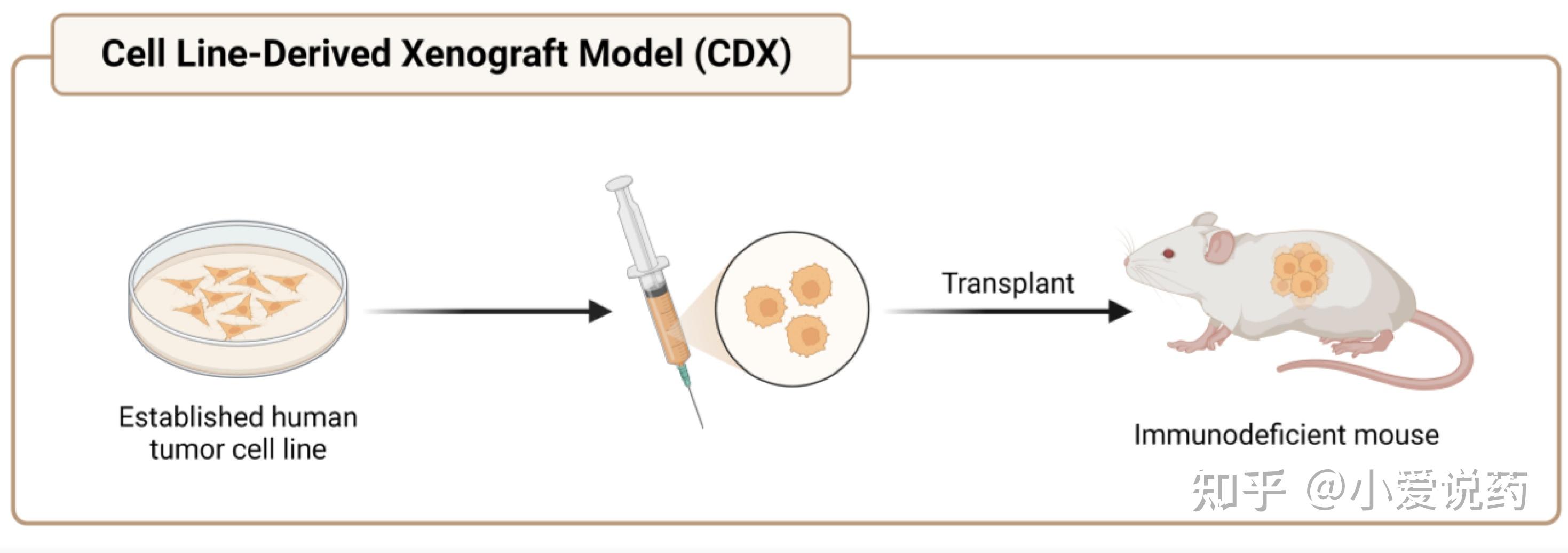
二、CDX 模型构建的标准化流程
2.1 细胞准备阶段:模型成功的首要前提
细胞质量直接决定 CDX 模型的成瘤率和稳定性。实验前需完成三项核心验证:STR 身份鉴定确保细胞系正确无误,支原体检测排除污染干扰,活力评估要求活细胞比例>95%。对于难成瘤细胞系,爱思益普采用体外成球培养或 Matrigel 预包被技术,显著提升细胞体内存活能力。
细胞接种密度需精准控制——皮下接种通常采用 5×10⁶-1×10⁷细胞/只,原位接种则根据组织特性调整至 1×10⁵-5×10⁶细胞/只。细胞悬液体积严格控制在 100-200μL,避免过量导致局部压力过大、细胞死亡。
2.2 动物接种阶段:品系匹配与操作规范
免疫缺陷小鼠的选择是 CDX 模型构建的核心决策。Nude 小鼠(裸鼠)适用于免疫原性较弱的实体瘤细胞系,成本低廉且饲养简单;NOD-SCID 小鼠 T/B 细胞双重缺陷,成瘤率较 Nude 小鼠提升 30% 以上,是大多数肿瘤细胞系的首选;NSG 小鼠(NOD-SCID-IL2Rγnull)免疫缺陷程度最高,完全缺失 T/B/NK 细胞,适用于血液肿瘤或需要长期观察的研究。
接种操作的技术细节直接影响成瘤效果。爱思益普技术团队通过优化进针角度(45°斜刺)、推注速度(缓慢均匀)和针道封闭(维持 10 秒后拔针),将细胞泄漏率控制在 5% 以下,成瘤成功率稳定在 90% 以上。
2.3 成瘤监测阶段:标准化观察体系
接种后第 3 天起建立每日触诊制度,记录成瘤潜伏期。肿瘤可触及后(通常直径 3-5mm),改用游标卡尺测量,体积计算公式为 V=0.5×长径×短径²。当肿瘤体积达到 100-200mm³时即进入药效评价窗口期,此时模型批间差异应<20%,确保后续药效数据的可靠性。
三、原位接种技术:模拟临床微环境的高级建模
相较于皮下接种,原位接种能更真实还原肿瘤与宿主组织的相互作用,为药物组织渗透性、微环境响应和转移潜能研究提供可靠平台。该技术对操作精度要求极高,需掌握三大核心要点。
术前准备需精准定位接种坐标。以肝癌原位模型为例,暴露小鼠肝左叶后,选择距肝缘 2mm、避开大血管的实质区域作为注射点。细胞悬液体积严格控制在 30-50μL,过量导致包膜下渗漏,过少影响成瘤率。爱思益普采用显微外科技术,在体视显微镜下完成操作,实现细胞的精准递送。
术中操作强调无菌与快速。开腹时间超过 10 分钟将显著增加术后感染风险,因此需提前预冷细胞悬液、预热手术器械。进针深度根据组织厚度调整——肝脏约 3-4mm,胰腺约 2-3mm,过深易损伤血管,过浅则形成皮下种植。
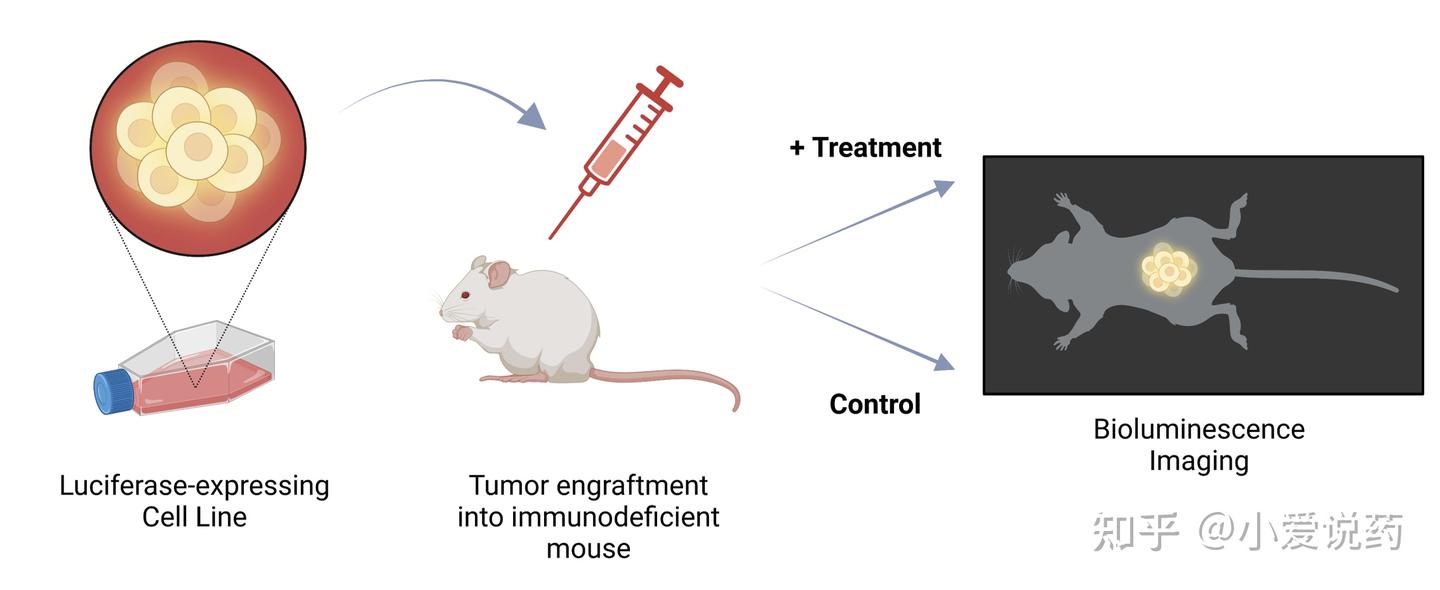
术后管理是模型成功的保障。原位接种术后需单独饲养 48 小时,提供软质饲料和温水。每日监测体重(下降>15% 需干预)和腹部体征。成瘤监测依赖影像学——超声检查可在接种后 7 天探测到早期病灶,生物发光成像(BLI)适用于荧光素酶标记细胞系的实时追踪。
爱思益普已建立肝、肺、胰腺、脑、骨等多器官原位接种 SOP,成瘤率稳定在 75-85%,为创新药物的组织特异性评价提供关键平台。
四、质量评价体系:三级质控确保数据可靠性
CDX 模型构建完成后,需通过系统化的质量评价确保其适用于后续药效研究。爱思益普建立的三级质控体系涵盖细胞级、动物级、组织级三个维度。
细胞级质控验证细胞身份和状态。STR 鉴定确认细胞系正确性,支原体 PCR 检测排除污染,流式细胞术验证靶抗原表达水平。对于基因编辑细胞系,需通过测序确认突变位点,Western Blot 验证蛋白表达变化。
动物级质控评估成瘤特性。记录成瘤潜伏期、生长曲线、成瘤率三项基础指标。优质 CDX 模型应具备潜伏期短(7-14 天)、生长速率适中(体积倍增时间 3-5 天)、批间差异小(CV<20%)的特点。若肿瘤生长过快(<7 天达评价体积),可能因坏死影响药效判断;生长过慢(>21 天)则延长实验周期、增加成本。
组织级质控确认肿瘤保真度。处死动物后取肿瘤组织进行 H&E 染色,观察细胞形态、核分裂象、坏死区域是否与原始细胞系一致。免疫组化检测 Ki-67(增殖指数)、CD31(血管密度)等指标,评估肿瘤生物学活性。对于特定瘤种,如乳腺癌需确认 ER/PR/HER2 状态,肺癌需保留驱动基因突变(EGFR、KRAS)。
通过三级质控的 CDX 模型,方可进入后续药效评价阶段,确保数据符合 IND 申报要求。
五、CDX 模型在创新药物研发中的应用场景
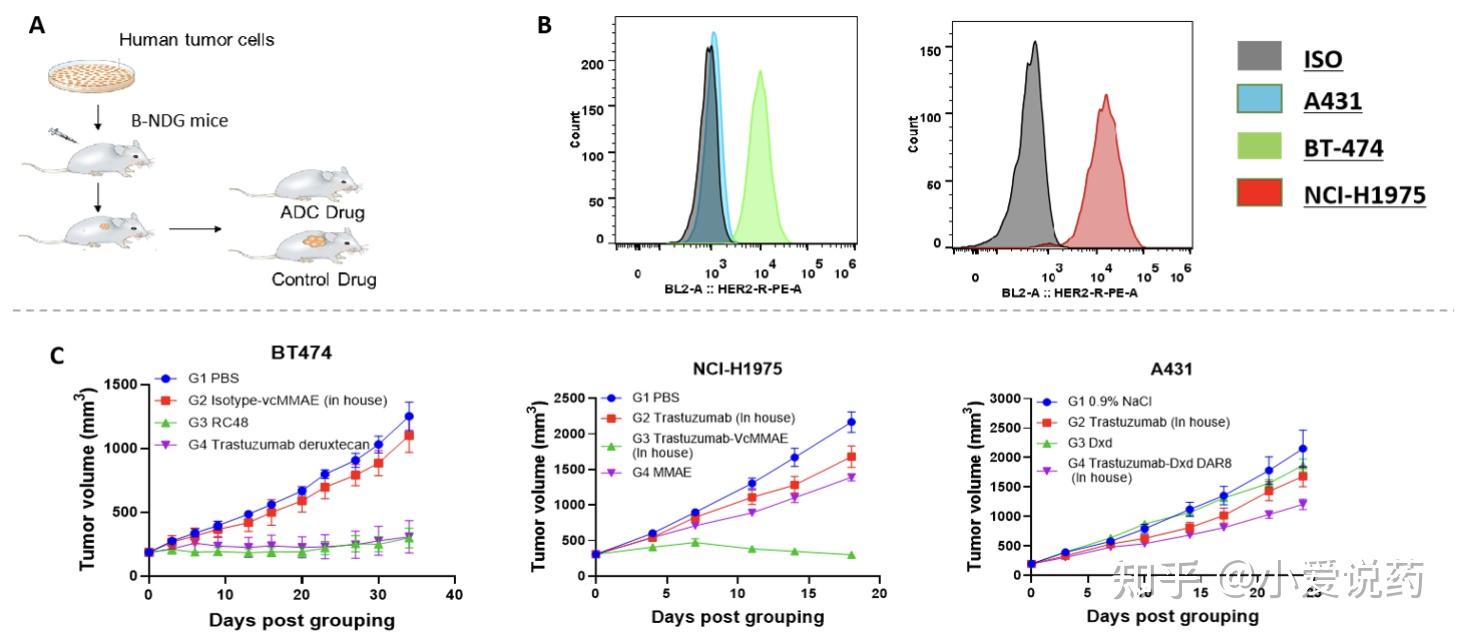
5.1 ADC 药物的体内评价平台
ADC(抗体偶联药物)的研发对 CDX 模型提出了特殊要求。作为靶向递送系统,ADC 需要模型同时具备靶抗原高表达、肿瘤可及性、免疫耐受性。爱思益普针对 ADC 药物开发了专用 CDX 模型库,涵盖 HER2、Trop2、CLDN18.2 等 20+靶抗原的高表达细胞系。
药效评价设计需考虑 ADC 独特机制。除常规肿瘤生长抑制率(TGI%)外,增加旁观者效应评估——在靶抗原阳性细胞中混入阴性细胞,评价 payload 是否杀伤邻近细胞。药代动力学研究同步进行,测定 ADC、总抗体、游离 payload 的血药浓度,计算肿瘤组织药物暴露量(AUCtumor/AUCplasma),为临床剂量预测提供依据。
5.2 靶向治疗与联合用药研究
CDX 模型是验证靶向药物作用机制的理想平台。通过选择携带特定驱动基因突变的细胞系(如 EGFR T790M、ALK 融合、BRAF V600E),可评价抑制剂的靶向活性和选择性。爱思益普建立的耐药 CDX 模型库,通过体外药物诱导或基因编辑技术,模拟临床获得性耐药场景,为下一代抑制剂开发提供评价工具。
联合用药研究利用 CDX 模型的标准化优势,设计严格的剂量-效应矩阵实验。通过 Bliss 独立模型或 Loewe 加和模型分析药物相互作用,筛选协同组合,为临床联合方案设计提供数据支撑。
5.3 免疫治疗药物的评价窗口
尽管 CDX 模型缺乏人源免疫系统,但通过人源化小鼠(PBMC 或 HSC 重建)或细胞因子转基因细胞系(如 IL-2、GM-CSF 分泌型),可部分重建免疫微环境,评价免疫检查点抑制剂、CAR-T 细胞等药物的体内活性。爱思益普的 NSG-hIL15 模型支持 NK 细胞重建,为 ADCC 机制研究提供独特平台。
六、技术展望与服务优势
随着肿瘤药物研发向精准化、联合化方向发展,CDX 模型构建服务也在不断升级。爱思益普的技术优势体现在三个维度:
💡模型资源丰富度:覆盖 100+人源肿瘤细胞系,涵盖肺癌、乳腺癌、结直肠癌、胃癌、血液肿瘤等主要瘤种,支持基因编辑和耐药模型定制。
💡技术平台整合度:将 CDX 模型与体外药效、DMPK、安全性评价整合,提供从靶点到 IND 的一站式服务,减少多供应商协调成本。
💡质量体系建设:通过 AAALAC 认证,建立符合 GLP 规范的实验流程,数据获 FDA、NMPA 认可,支持全球申报。
CDX 动物模型构建服务作为临床前研究的基石,其技术成熟度、数据可靠性和服务专业性,直接影响创新药物的转化效率。选择具备完善技术体系和丰富项目经验的 CRO 合作伙伴,是制药企业加速研发进程、降低开发风险的关键决策。

扫一扫关注
爱思益普公众号


业务咨询
北京
业务咨询专线:010-6780-9840
联系地址:北京市经济技术开发区科创十三街18号院锋创科技园16号楼
上海
业务咨询专线:010-6780-9840
联系地址:上海市浦东新区蔡伦路780号新技术推广大楼3E5O室
徐州
业务咨询专线:010-6780-9840
联系地址:江苏省徐州市云龙区淮海文博园 二号楼2层
贵州
业务咨询专线:010-6780-9840
联系地址:贵州省贵阳市南明区龙岭路50号 欧美医药产业园一期2号楼



