News Detail
 来源:2026-05-07 09:01:30
来源:2026-05-07 09:01:30
 浏览量:11167
浏览量:11167
一种化合物在试管里能杀死癌细胞,不代表它能成为药物。关键问题在于:它进入人体后,有多少能被吸收?进入血液后分布到哪些器官?在肝脏里被代谢成什么?最终通过肾脏还是胆汁排出?这些问题的答案,决定了这个化合物能否成药。
这就是药代动力学(DMPK)研究的核心——描绘药物在体内的「路线图」。历史上,大量候选药物因药代性质不佳而折戟:口服后几乎不被吸收、在体内半衰期太短需要一天注射三次,或者代谢产物具有意想不到的毒性。这些失败往往发生在研发后期,代价极其高昂。
爱思益普的 DMPK 平台,正是围绕这套「路线图」构建的。从体外 ADME 筛选到体内药代动力学研究,平台覆盖了药物研发从先导化合物优化到临床前申报的全流程 。
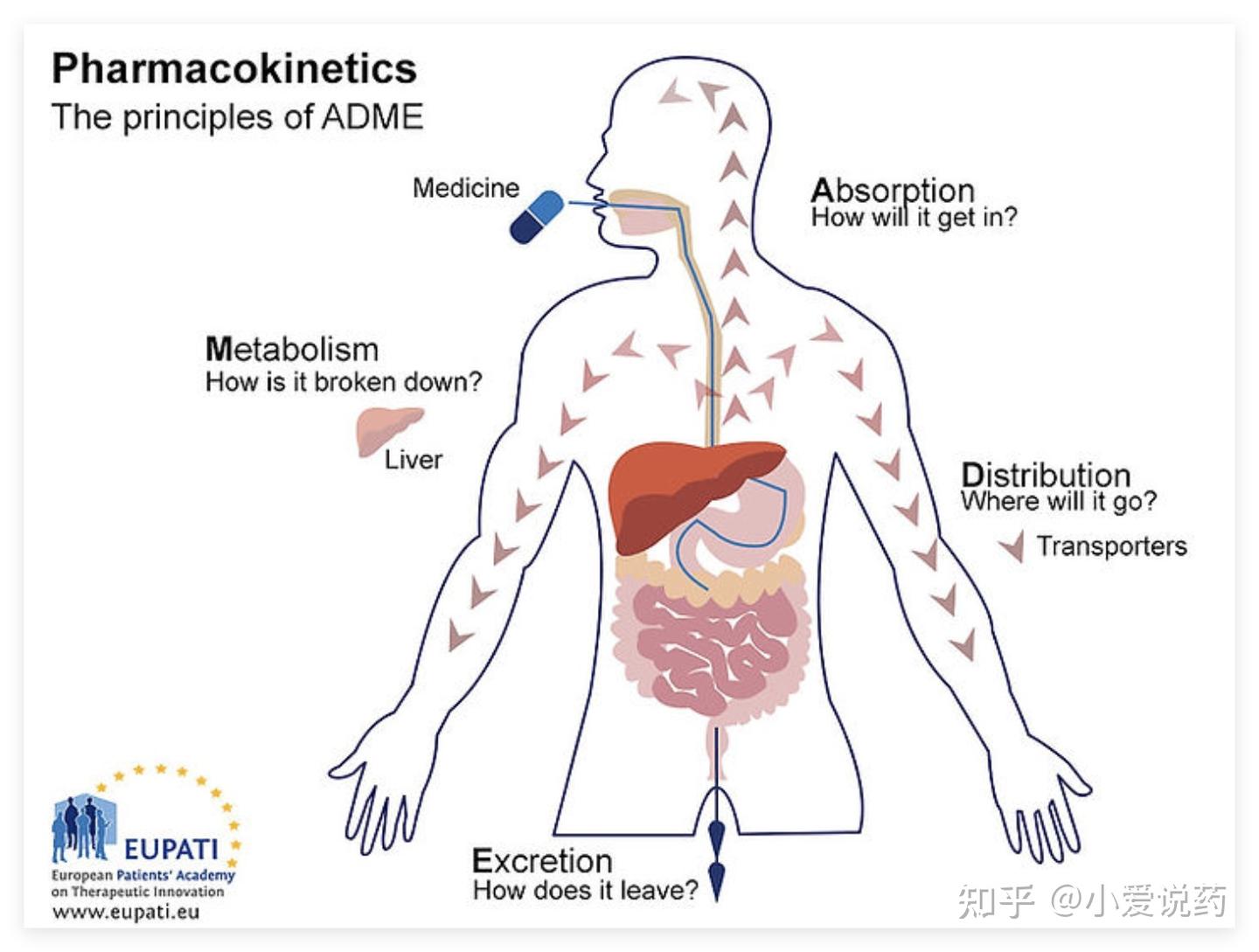
⭐ 第一级:快速画像。 包括溶解度、渗透性、血浆蛋白结合率、内在清除率、亲脂性等基础参数。这些指标用 LC-MS/MS 技术检测,可以在几天内完成,帮助客户判断一个化合物是否具备「可成药性」的基本条件。例如,溶解度太差的化合物,口服后难以被吸收;渗透性太低的化合物,难以穿过肠道屏障进入血液。
⭐ 第二级:深度解析。 在第一级基础上,进一步研究代谢途径、代谢产物鉴定、药物相互作用潜力、转运体介导的摄取/外排等。这部分需要更复杂的实验设计,比如用肝微粒体、肝细胞或重组酶系孵育化合物,分析其代谢产物结构和生成速率 。
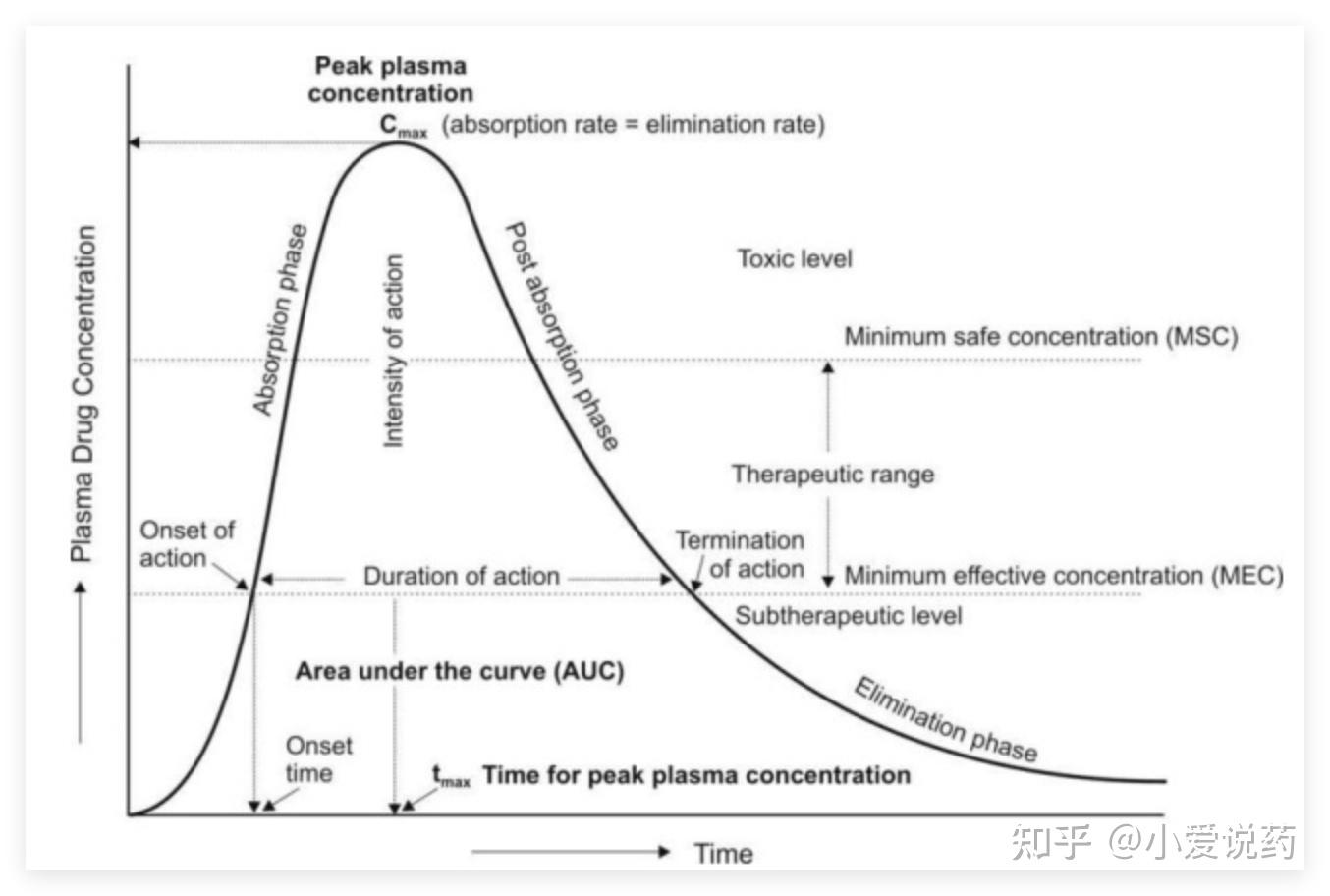
一个实际的案例:在某抗肿瘤药物研发中,平台通过肝微粒体孵育实验发现,候选分子在人体肝微粒体中的半衰期较动物模型延长 3 倍,且主要代谢产物无毒性风险。这个数据直接影响了临床试验的给药方案设计——如果按动物数据设计剂量,人体中可能出现药物蓄积导致毒性;而体外数据提前预警了这种差异 。
这种「体外排雷」策略,可以将研发失败的风险前置到早期阶段,避免后期更大的损失。
中枢神经系统(CNS)药物研发的最大瓶颈之一,是血脑屏障(BBB)。这层由脑微血管内皮细胞、周细胞和星形胶质细胞共同构成的“生物城墙”,阻挡了绝大多数药物进入大脑。一种化合物即使在外周表现出优异的活性,如果不能穿过血脑屏障,就无法治疗脑部疾病。
爱思益普的 BBB 模型平台,采用人源细胞共培养体系,结合跨膜电阻(TEER)监测与荧光标记示踪技术,模拟 BBB 的生理屏障特性 。通过测量药物穿透屏障的速率和程度,可以预判其在脑组织中的暴露水平。
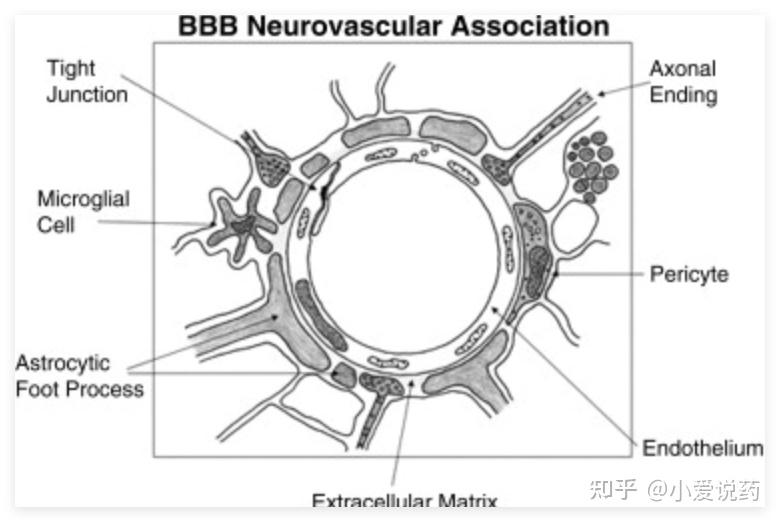
在帕金森病药物研发中,平台通过 BBB 模型筛选出可高效通过屏障的候选分子,临床前数据显示其脑内药物浓度较传统制剂提升数倍 。在抗阿尔茨海默病药物研发中,平台结合 BBB 模型与酶活性检测,筛选出的候选分子脑内浓度较传统药物提升 3 倍,且无明显脱靶效应 。
这个模型的价值不仅在于「筛选」,更在于「指导优化」。如果一种化合物 BBB 穿透率不理想,可以通过结构修饰或纳米载体递送系统来改善。平台已为多家企业提供了这类定制化解决方案。
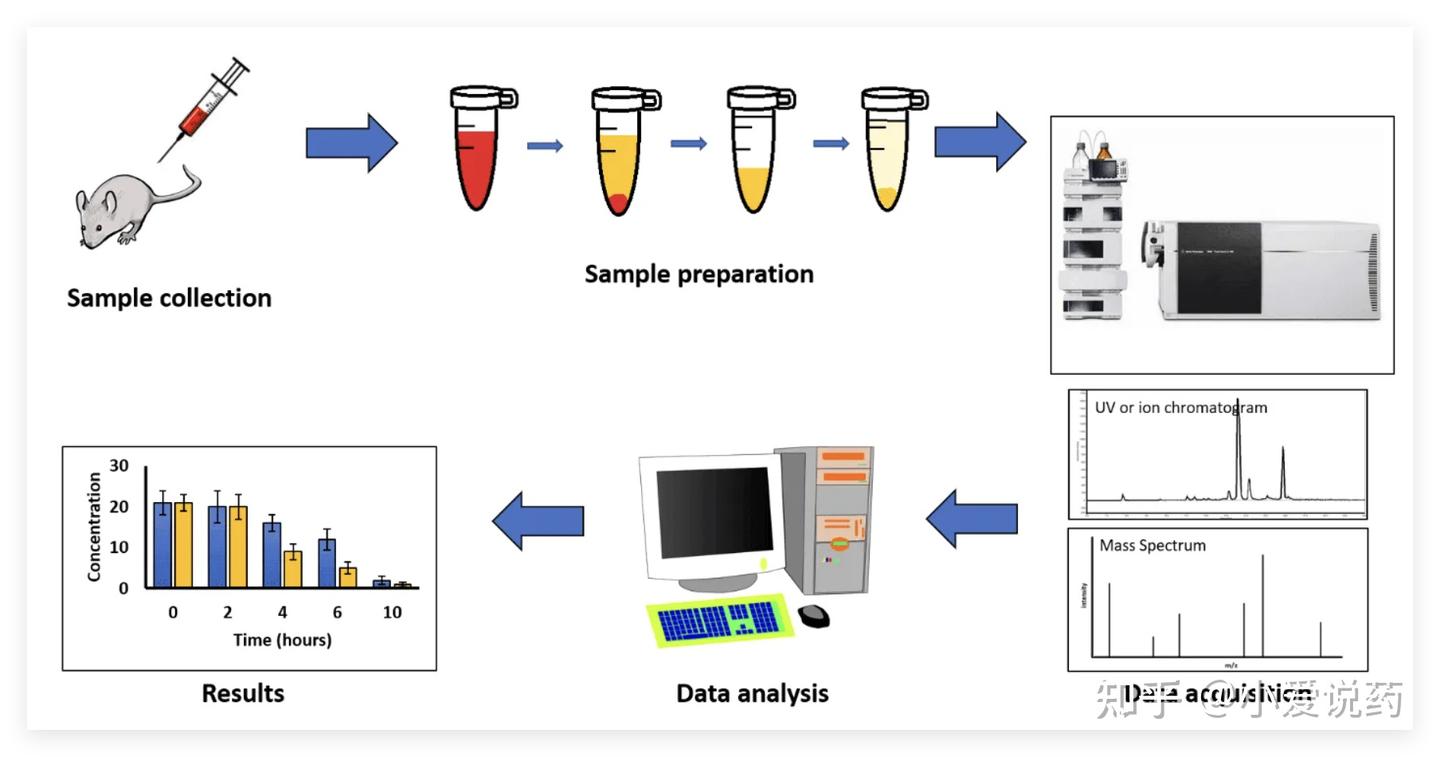
体外数据再漂亮,最终也要在体内验证。爱思益普的体内药代动力学研究,覆盖小鼠、大鼠、犬、猴等多种实验动物,支持静脉注射、口服、皮下注射等多种给药途径 。
样本采集环节的设计尤为关键。不同给药途径、不同化合物,其吸收和分布特征差异巨大。平台针对不同场景设计时间梯度采样方案,确保覆盖药物代谢的关键节点。例如,在抗癫痫药物研发中,团队每 15 分钟采集一次血液样本,结合微透析技术实时监测脑脊液药物浓度,完整捕捉了药物的动态分布特征 。
样本处理采用模块化设计:
🖥️ 血液样本通过离心分离血浆后,利用固相萃取技术去除内源性干扰物,回收率稳定在 95% 以上;
🖥️ 尿液样本通过 pH 调节与有机溶剂沉淀结合,实现代谢产物的富集;
🖥️ 脑组织样本则通过优化超声破碎参数,将目标化合物提取效率提升至 82% 。
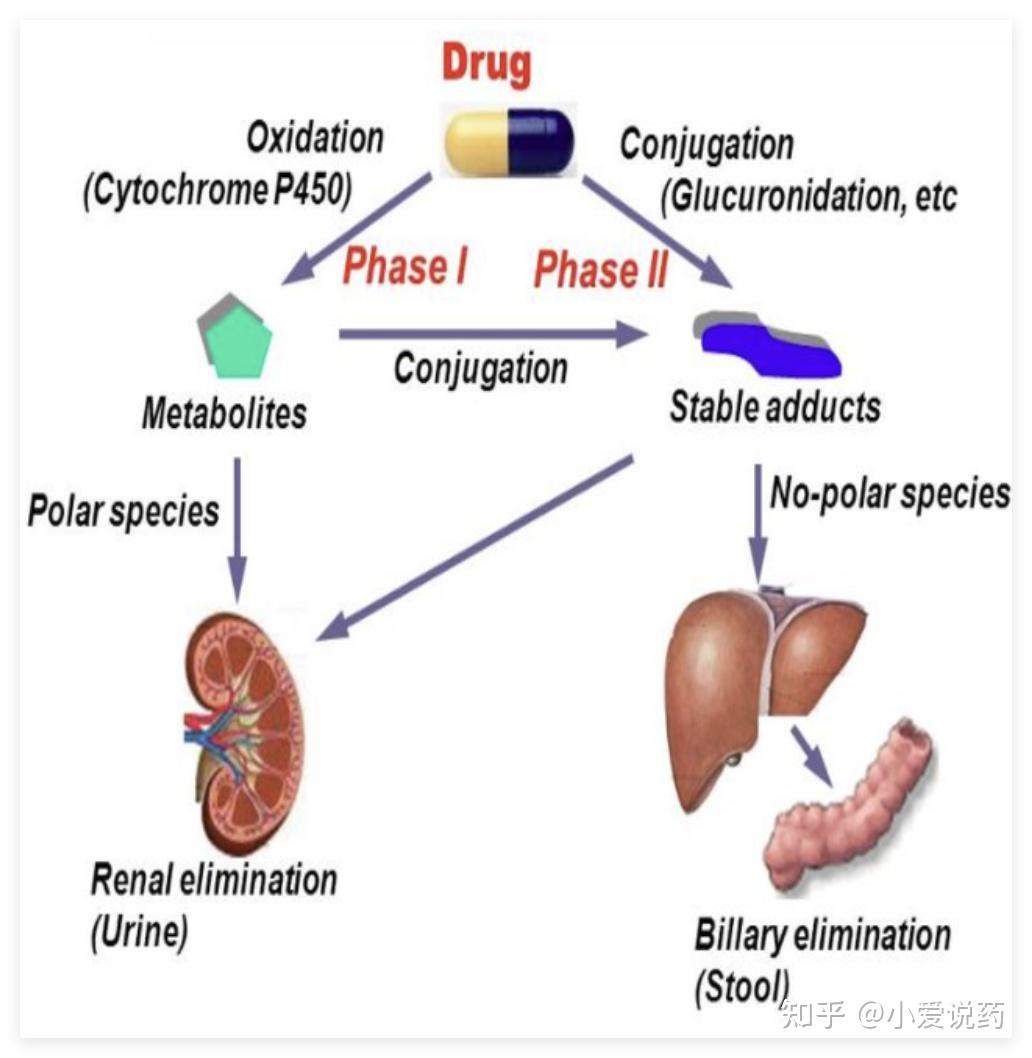
数据分析依托专业软件(如 Phoenix WinNonlin、GastroPlus),通过非房室模型与房室模型的联合应用,计算半衰期、生物利用度、分布容积等关键参数。在某抑制剂研发中,模型预测其脑组织暴露量与实际动物实验数据的误差小于 6%,为剂量设计提供了科学依据 。
抗体药物、ADC(抗体偶联药物)、小核酸药物等大分子疗法,正在改变药物研发的格局。但它们的药代动力学特征与小分子化学药截然不同:分子量大、不能口服、主要通过网状内皮系统清除、存在免疫原性风险。
爱思益普的大分子及 ADC 药物筛选评价平台,整合了从分子水平、细胞水平到动物模型的完整 DMPK 评价能力 。这包括 payload(细胞毒素)的筛选评价、ADC 生物学评价、生物分析方法开发、DMPK 研究方案设计及结果解读、免疫原性评价和体内药理药效研究等综合服务。
在 ADC 的 DMPK 研究中,一个核心挑战是同时追踪抗体部分和小分子毒素部分的命运。平台采用 LC-HRMS 方法,能够识别 ADC 释放的未知小分子,监测药物抗体比(DAR)的变化和血浆稳定性,这些参数直接影响 ADC 的疗效和安全性 。
对于单克隆抗体,平台建立了基于 LC-MS/MS 的定量分析方法,与传统 ELISA 技术相比,具有更高的特异性和更短的方法开发周期。在曲妥珠单抗的 PK 研究中,LC-MS/MS 结果与 ELISA 结果无系统性偏差,但灵敏度更高、样品处理更简便 。
☂️ 样本管理: 从采集、运输、存储到处理,每个环节都有标准化流程。关键设备定期接受第三方校准并保留证书。
☂️ 检测精度: 通过优化样本处理流程与检测灵敏度,将误差控制在 5% 以内。在组织分布研究中,单次实验能同步获取药物在血浆及多种组织中的浓度数据 。
☂️ 数据追溯: 采用专业软件构建药代动力学模型,所有原始数据、处理参数、计算结果均可追溯,满足监管申报要求。
☂️ 报告规范: 提供中英文双语报告,支持中美双报需求。截至 2025 年,平台已支持 50 余个项目的药代动力学研究,其中 15 个项目进入临床阶段 。
传统 CRO 的服务模式是「按项目收费」——客户送来化合物,CRO 完成检测,交付报告,项目结束。但这种模式在复杂的 DMPK 研究中存在明显局限:一个化合物的药代特征,往往需要多轮实验、多种模型、多个物种的数据才能完整描绘。
爱思益普提出的「CRO+」概念,在 DMPK 领域的体现是「一体化服务」。从早期的体外 ADME 筛选、到中期的体内 PK 研究、再到后期的代谢产物鉴定和药物相互作用评估,提供连续性的技术支持。客户不需要在多个供应商之间协调,也避免了数据在不同环节衔接时的信息损耗。对于长期合作项目,FTE模式可以提供更稳定的团队支持和更深入的技术参与;对于短期项目,FFS模式则更灵活。此外,平台支持 FTE(全职 equivalent)和 FFS(按服务收费)两种合作模式。
药物研发是一项高投入、高风险、长周期的系统工程。DMPK 研究的价值,在于用相对可控的体外和动物实验成本,规避后期临床试验中不可控的失败风险。
从爱思益普 DMPK 平台十五年的发展来看,其核心能力可以概括为三个层面:
💡 一是技术平台的完整性——从体外 ADME 到体内 PK,从小分子到大分子,覆盖主要药物形态;
💡 二是数据质量的可靠性——严格的质控体系、可追溯的数据管理、满足申报要求的报告规范;
💡 三是服务模式的灵活性——根据项目需求定制方案,支持不同合作模式。
对于创新药企而言,选择 DMPK 合作伙伴时,不应只关注“能不能做某项检测”或“价格是否便宜”,而应考察其技术链条的完整性、数据质量的稳定性,以及是否有支持药物进入临床的成功案例。因为这些因素,最终决定了体外数据能否可靠地预测人体表现——而这,正是药物研发中最昂贵的决策依据。

扫一扫关注
爱思益普公众号


业务咨询
北京
业务咨询专线:010-6780-9840
联系地址:北京市经济技术开发区科创十三街18号院锋创科技园16号楼
上海
业务咨询专线:010-6780-9840
联系地址:上海市浦东新区蔡伦路780号新技术推广大楼3E5O室
徐州
业务咨询专线:010-6780-9840
联系地址:江苏省徐州市云龙区淮海文博园 二号楼2层
贵州
业务咨询专线:010-6780-9840
联系地址:贵州省贵阳市南明区龙岭路50号 欧美医药产业园一期2号楼



