News Detail
 来源:2024-03-26 09:47:06
来源:2024-03-26 09:47:06
 浏览量:17479
浏览量:17479
爱求索、思新异、益中国、普创新。
为鼓励大家跟踪前沿专利和文献,工作中保持积极学习的心态,员工自发组织了《每周一文》系列文章,旨在阅读并梳理文章中的关键技术和结果,结合公司的新药研发平台,寻求拓展,希望能助力更多创新的研究团队,支持“产学研医药”大融合。

肥胖是全球关注的健康话题,过度肥胖和肥胖相关的并发症包括2型糖尿病(T2D)、心血管疾病、骨关节炎、阻塞性睡眠呼吸暂停和多种癌症等,是全球患病和死亡的主要原因之一。控制超重可以改善代谢健康,延缓肥胖相关合并症的进展。最近研究表明,在T2D患者中,与选择性GLP-1R激动剂相比,葡萄糖依赖性促胰岛素多肽受体(GIPR)和GLP-1R双受体激动剂Tirzepatide显示出减轻体重的现象。与GLP-1R单激动剂相比, GLP-1R和GCGR双激动剂JNJ-64565111、BI 456906和Pemvidutide对体重减轻显示出更大的潜力。考虑到GIPR和GLP-1R双激动剂Tirzepatide以及GLP-1R和GCGR双激动剂的优势,靶向GIPR,GLP-1R和GCGR三受体的三重激动剂有可能提供一种新的治疗策略,与单受体和双受体激动剂相比,三重激动剂会显示更好的血糖控制及减肥效果。在临床前模型中,降低三种受体活性导致体重减轻的效果比任何双受体激动剂都要显著[1]。最近,首次报道了一种三激动剂的在病人中的治疗结果[2]。
在Tamer Coskun等人2022年发表的文章《LY3437943, a novel triple glucagon, GIP, and GLP-1 receptor agonist for glycemic control and weight loss: From discovery to clinical proof of concept》中,提出了LY3437943 (LY)(图1A)化合物,是一种由GIP肽主链改造而成脂肪酸酰化的单肽,在GCGR、GIPR和GLP-1R上具有三重激动剂的活性,通过调节GCGR、GIPR和GLP-1R的活性对代谢产生益处。
该文首先在临床前模型中研究了LY的药理学和作用机制。在体外模型的研究中,使用表达人GCGR、GIPR或GLP-1R的HEK-293细胞系来检测受体激活下游第二信使3',5'-环腺苷单磷酸(cAMP)含量。在人GCGR中,LY的效力是人源Glucagon的2.9倍(LY 的EC50为5.79 nM,而人源Glucagon的 EC50为1.97 nM)(图1B)。LY在人GIPR中显示出比GIP(1-42)NH2高8.9倍的效力(LY的EC50为0.0643 nM,人类GIP(1-4)NH2的EC50为0.574 nM)(图1C)。在人GLP-1R中,LY的效力是GLP1(7-36)NH2的2.5倍(LY 的EC50为0.775 nM,而人GLP-1(7-36)NH2的EC50为0.312 nM)(图1D)。功能实验结果表明,LY是GCGR、GIPR和GLP-1R的完全激动剂。此外,本文还进一步探索了LY在人的内源性表达GIPR或GCGR细胞模型中的体外活性,研究了优先表达GIPR的分化人脂肪细胞和优先表达GCGR的人诱导多能干细胞源性肝细胞的功能。结果显示,在肝细胞中,LY在刺激葡萄糖产生方面与天然Glucagon具有相似的效力(图1E)。在脂肪细胞中,LY比天然GIP更能促进脂肪分解(图1F)。综上所述,体外研究结果表明,LY是人GCGR、GIPR和GLP-1R的强效激动剂。
在体内模型的研究中,采用多种转基因小鼠模型来评估受体对营养和能量代谢的影响。为了评估LY对GIPR和GLP1R活性,使用腹膜内葡萄糖耐量试验(ipGTT)在野生型、GIPR敲除小鼠(GIPr-/-)和GLP-1R 敲除小鼠(GLP1r-/-)中评估体内血糖控制水平。与Semaglutide和长效GIP类似,LY治疗改善了上述3种基因型的葡萄糖偏移(图1G-1I),LY可以通过GIP或GLP-1受体改善ipGTT中的葡萄糖耐受性。为了评估胰高血糖素活性,研究者通过在LY给药前24小时用GIPR抗体拮抗剂治疗GLP-1R敲除小鼠来阻断GIPR和GLP-1R活性。在小鼠缺乏GIPR和GLP-1R的情况下,LY在给药1小时后增加了血糖水平,当用GCGR抗体拮抗剂预处理后阻断了葡萄糖的增加,证明LY在体内具有激活GCGR的功能,在没有GIPR和GLP1R激动剂的情况下可以增加血糖水平(图1J)。

图1 LY3437943是一种GCGR/GIPR/GLP-1R三重激动剂
接下来,为了研究LY对体重、能量代谢、身体成分和肝脂肪变性的影响,对C57/Bl6饮食诱导的肥胖(DIO)小鼠注射LY。结果显示, LY降低了小鼠体重(图2A和2C)和卡路里摄入量(图2B) ,并呈现出剂量依赖性。体重的减少主要是与脂肪量的减少(图2D)相关,对瘦体量的影响很小(图2E)。LY通过降低了血糖含量和血浆胰岛素含量(图2G和2H),改善了血糖控制,同时对胰岛素敏感性也有改善,这与双GIPR/GLP-1R激动作用的结果一致。此外,血浆丙氨酸转氨酶和肝脏甘油三酯的降低也表明LY对肝脏健康有所改善(图2I和2J)。
在另一项实验中测试了LY与Tirzepatide对肥胖小鼠体重减轻的效果。结果显示在肥胖小鼠中,当每天以10 nmol/kg的剂量治疗时,LY与Tirzepatide相比,能促进体重减轻(图2K),且与更多的卡路里摄入量减少有关(图2L),这可能是LY具有强效减肥作用的部分原因。
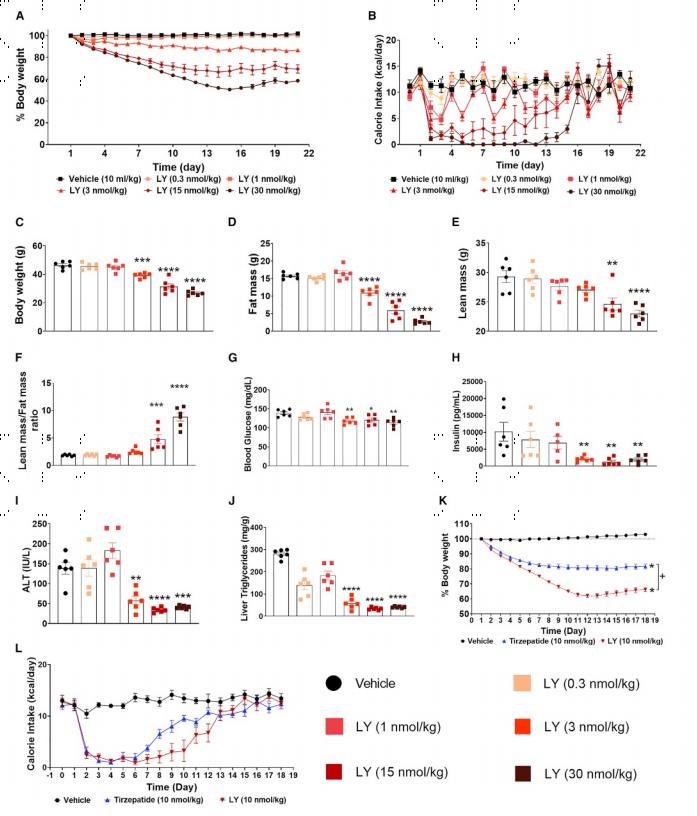
图2 降低饮食诱导的肥胖小鼠的体重并改善其代谢健康
为了阐明这一点,研究者对LY进行了进一步的研究。通过检测LY处理高脂诱导的肥胖小鼠后的体重百分比(图3A)、卡路里摄入量(图3B)、能量消耗(图3B)、能量平衡(图3D)、呼吸交换率(图3E)、运动活性(图3F)、以及身体成分等指标相对于基线的变化(图3G和3H)情况,以此来评估能量消耗对减肥的影响,证明GCGR激动作用是消耗能量的关键因素(图3I和3K)。
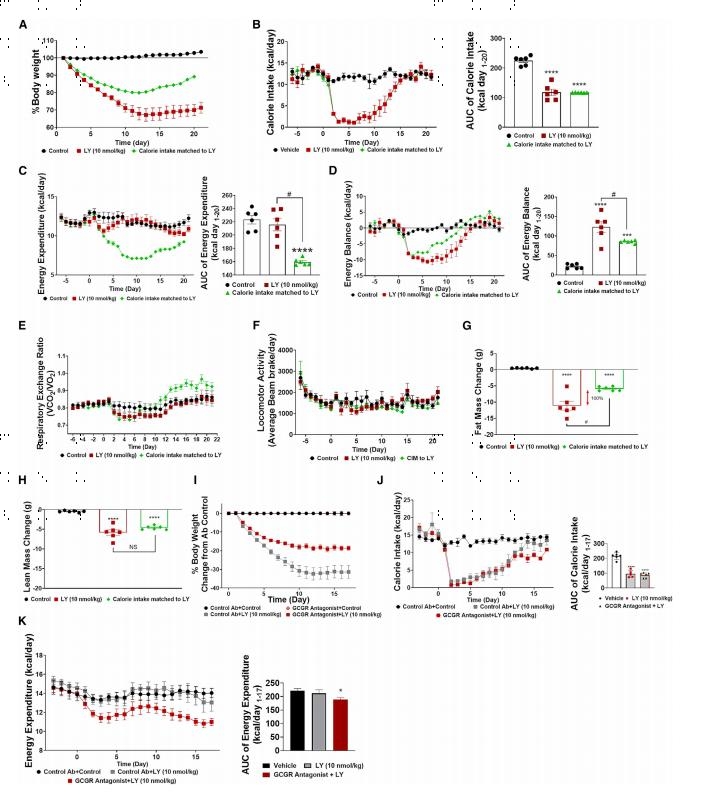
图3 LY3437943中胰高血糖素受体激动作用导致肥胖小鼠能量消耗增加
最后,研究者首次在人类1期研究中进行单次递增剂量实验来评估LY的安全性和药物代谢动力学(PK)。此次共有47名健康参与者参与了该研究,其中45人至少接受了1剂LY或安慰剂,2人在第一剂随机治疗前停药(图4A)。表1总结了基于在整个剂量范围内测得的LY血浆浓度的非室PK参数。在给药后12–72小时内观察到的最大LY浓度(图4B),LY的PK在所研究的剂量范围内几乎呈剂量比例,单次递增LY剂量给药后,从基线到第43天的空腹血糖平均变化与安慰剂相比并不显著,这在非糖尿病患者中是意料之中的(图4E)。同时,观察到空腹平均胰岛素(图4F)和空腹C肽(图4G)较基线剂量平均水平有所增加,在给药后第2天和第3天(分别为24和48小时)达到最大水平;平均空腹C肽和胰岛素水平分别在第8天和第15天恢复到接近基线水平(图4F和4G)。在以4.5mg和6.0 mg的最高LY剂量水平给药后,从给药后24小时到第15天,观察到平均空腹胰高血糖素下降(图4H)。在这些指标中,观察到的下降幅度约为给药前水平的50%-75%,与GLP-1R和GCGR靶点作用一致。
除最低剂量0.1 mg外,其余所有剂量的LY治疗后,平均体重与基线相比均有下降(图4C),在最高剂量水平3-6 mg时,体重下降幅度最大。食欲视觉模拟评分(VAS)测试的结果能够更好地了解LY给药后的食欲,总体VAS评分越高表示食欲越低。虽然安慰剂或0.1 mg剂量的LY治疗后VAS评分没有变化,但0.3 mg或更高剂量的LY导致食欲VAS评分从基线开始总体增加(食欲下降),并且这些增加在给药后第2天和第3天最高(图4D)。
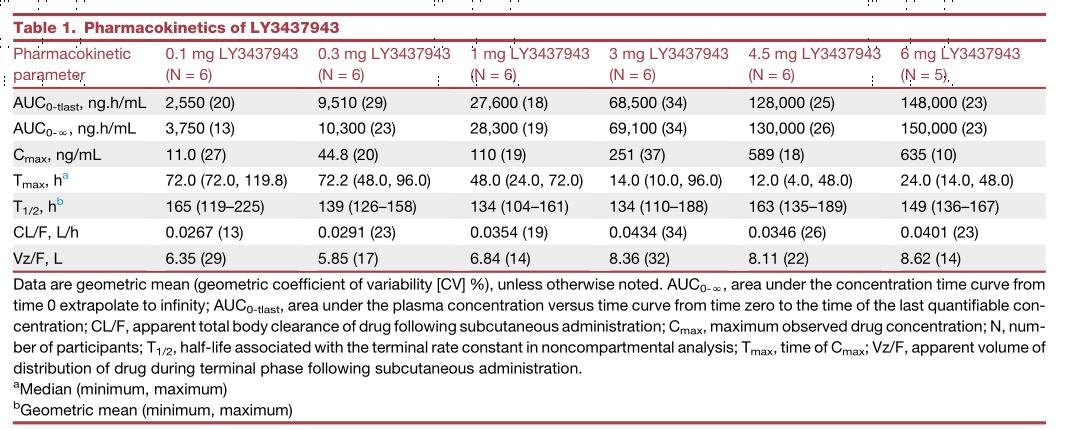
表1 LY3437943的药代动力学

图4 LY3437943在健康参与者的1期单次递增剂量临床研究
总体而言,在所有参与者中, 有44名(97.8%)受试者发生了治疗突发不良事件(TEAE),其中23名(51.1%)出现与研究治疗相关的TEAE,本研究期间未发生死亡或其他严重不良事件。随着LY剂量的增加,与研究治疗相关的TEAEs的参与者比例从16.7%增加到100%,而安慰剂组为30%。研究治疗相关TEAEs最常报道的是胃肠道疾病,包括呕吐、腹胀和恶心等症状。大多数TEAEs是轻微的,4.5 mg LY剂量组有2名参与者报告了6例中度TEAEs(呕吐和恶心)。
综上,LY具有不平衡的GIPR活性(有利于GIPR活性)和平衡的GCGR和GLP-1R活性。LY使肥胖小鼠的体重减轻了45%,具有降血糖功效,并改善了胰岛素抵抗。在单次递增剂量研究中,健康参与者显示LY耐受性良好。单次给药后的体重减轻一直维持到给药后第43天,食欲最初有所下降。在这项研究中,LY的安全性、耐受性和有效性结果支持对肥胖(NCTO4881760)和T2D(NCT04867785)参与者多次递增剂量LY的评估。
爱思益普研发团队构建了分别表达GLP-1R、GIPR或GCGR蛋白的CHO稳转细胞系,通过cAMP实验检测激动剂或拮抗剂对GLP-1R、GIPR及GCGR的激活或抑制情况,前期验证的 EC50值和IC50如下图展示:

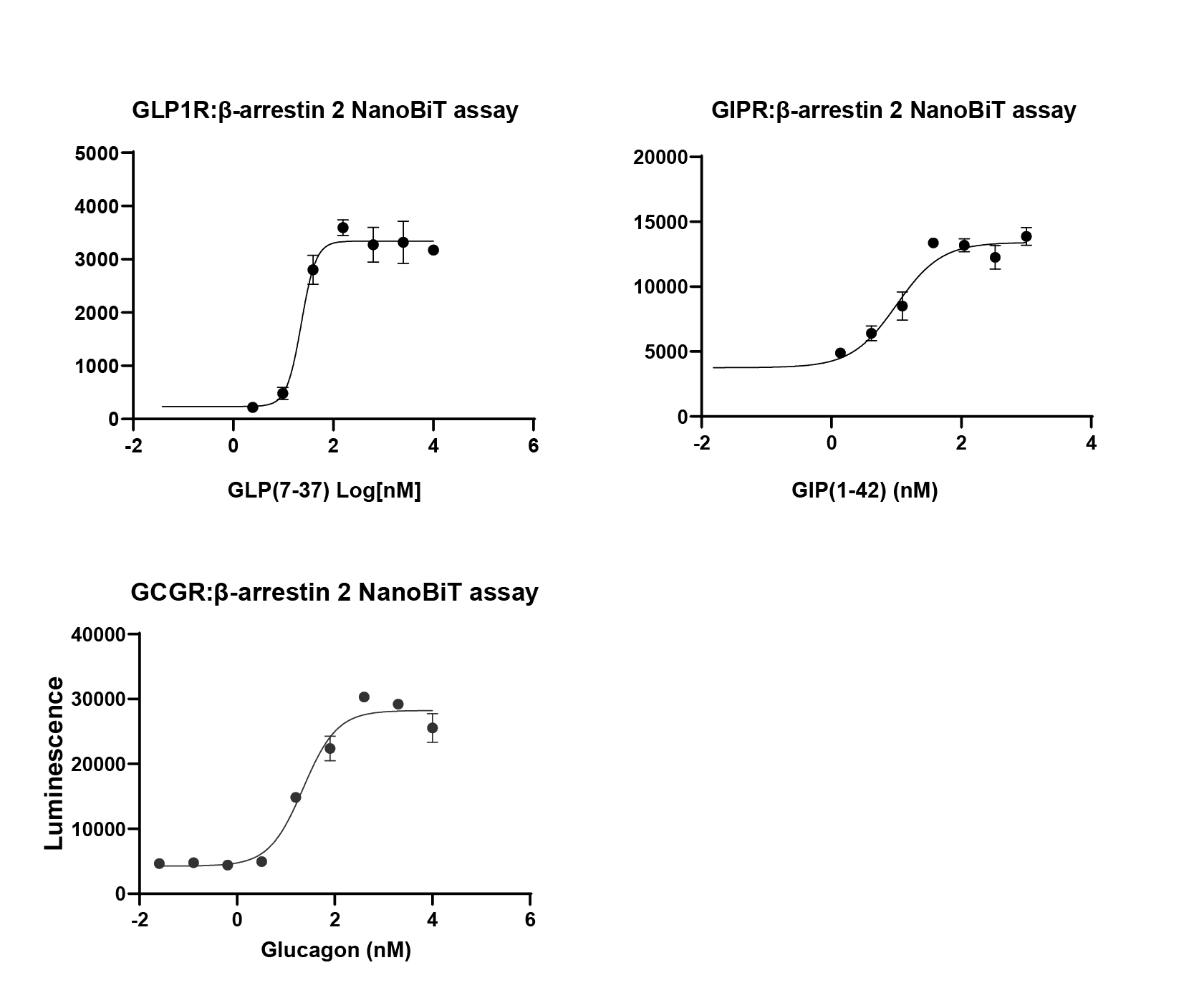
图2 GLP-1R、GIPR以及GCGR 的β-Arrestin NanoBit assay 验证数据
爱思益普研发团队构建优化了GLP-1R 的表面等离子共振现象(Surface Plasmon Resonance,SPR) Binding实验,非常灵敏的实时监测两个分子之间的结合/互作,且可进行高通量筛选操作。结果见图3:
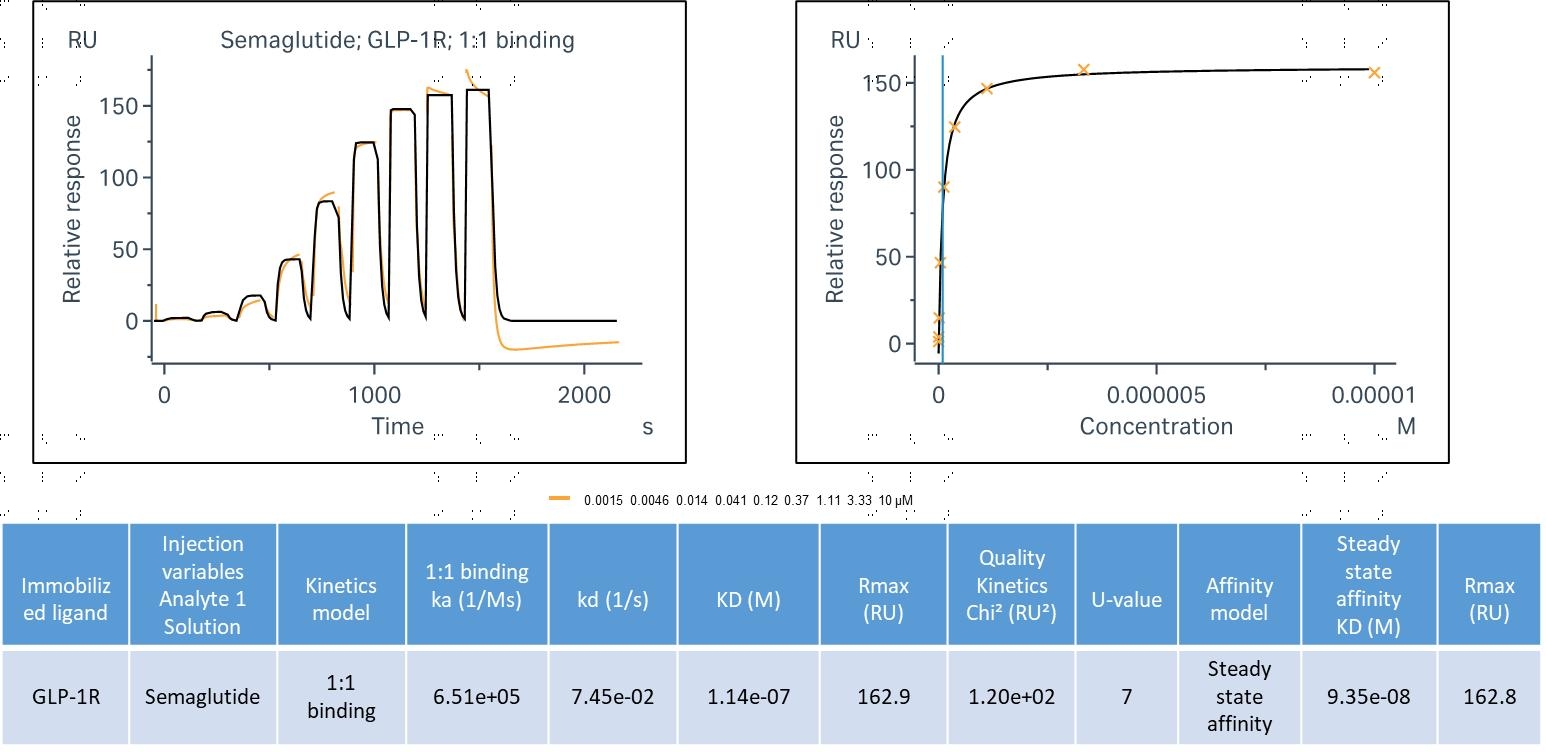
图3 GLP-1R SPR Binding assay 验证数据
北京爱思益普生物科技股份有限公司(ICE Bioscience InC.)专注于从先导化合物到临床前候选药物的生物学研发阶段,基于生化、细胞、体内模型、安全性评价等筛选技术和早期药物的机理研究,致力于建立全面的靶标筛选平台。
同时,爱思益普拥有一流的实验设备平台,包括AKTA (x3)、Biacore 8K、PHERAstar FSX、FLIPR、FACS、CLARIOstar PLUS、Echo 655、xevo TQ-GC、IVIS Lumina III、AB SCIEX 5500、Neon (x4)、LICOR、ChemiDoc和Operetta等,可结合HCS、Western Blot、qPCR、LC-MS、MSD多种研发技术,助力靶点的精准分析和验证。此外,爱思益普可以提供数百种肿瘤细胞及其他靶点的细胞系,在实验中也积累了大量的研发经验,为后期糖尿病和肥胖症靶向药物的开发及优化提供坚实的基础。
爱思益普团队走在药品研发科技领域的前沿,深入研究靶点药物的作用机理并时刻关注着药品研发的最新动向,以优质的服务和科技的创新为根本,不断优化试验策略,不断创新科研技巧,竭诚为国内外客户提供研发和检测服务,加速中国新药研发项目的进程。
[1] Finan B , Yang B , Ottaway N ,et al.A rationally designed monomeric peptide triagonist corrects obesity and diabetes in rodents[J].Nature Medicine[2024-02-28].DOI:10.1038/nm.3761.
[2] Bossart M , Wagner M , Elvert R ,et al. Effects on weight loss and glycemic control with SAR441255, a potent unimolecular peptide GLP-1/GIP/GCG receptor triagonist[J].Cell metabolism, 2022, 34(1):59-74.e10.

扫一扫关注
爱思益普公众号


业务咨询
北京
业务咨询专线:010-6780-9840
联系地址:北京市经济技术开发区科创十三街18号院锋创科技园16号楼
上海
业务咨询专线:010-6780-9840
联系地址:上海市浦东新区蔡伦路780号新技术推广大楼3E5O室
徐州
业务咨询专线:010-6780-9840
联系地址:江苏省徐州市云龙区淮海文博园 二号楼2层
贵州
业务咨询专线:010-6780-9840
联系地址:贵州省贵阳市南明区龙岭路50号 欧美医药产业园一期2号楼



