News Detail
 来源:2024-09-13 15:34:29
来源:2024-09-13 15:34:29
 浏览量:17133
浏览量:17133

一、蛋白质精氨酸甲基转移酶5 (PRMT5)与甲基-5'-硫腺苷磷酸化酶 (MTAP)介绍
PRMT5 (蛋白精氨酸N-甲基转移酶5) 是一种是一种甲基体蛋白质50 (MEP50) 辅因子依赖性甲基转移酶,它使用S-腺苷-1-甲硫氨酸 (SAM) 作为甲基供体,介导H2AR3 (H2AR3me2s) 和H4R3( H4R3me2s) 的双重对称二甲基化[1],这种修饰通过降低H4K5ac的水平有助于转录抑制[2]。此外,PRMT5介导的H3R8甲基化 (H3R8me2s) 也参与转录抑制[3]。PRMT5介导的H3R2甲基化 (H3R2me2s) 被WD重复序列5 (WDR) 的WD40结构域识别,并促进染色质上H3K4 (H3K4me) 的三甲基化 (图1)。这种机制诱导转录激活[4],从而调节多种重要的细胞功能。PRMT5在一系列癌症中过表达,包括结直肠癌、血液肿瘤和肺癌[5];
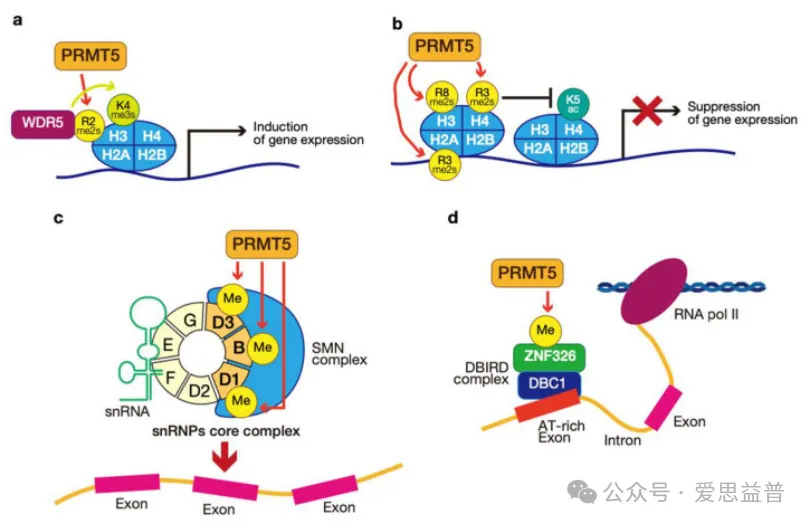
图1:蛋白质精氨酸甲基转移酶5 (PRMT5) 的作用。a,b:PRMT5介导的基因表达表观遗传调控的示意图。c,d:PRMT5介导的信使核糖核酸剪接机制[6]。
甲基-5'-硫腺苷磷酸化酶 (MTAP) 由位于第9号染色体上的甲硫腺苷磷酸化酶 (MTAP) 基因编码,催化甲硫腺苷 (MTA) 可逆的磷酸化为腺嘌呤和5-甲硫核糖-1-磷酸。蛋白质精氨酸甲基转移酶5 (PRMT5) 是MTAP缺失 (MTAP del) 癌症的合成致死靶点。该基因与最常缺失的肿瘤抑制基因CDKN2A相邻,且在人类癌症中频繁发生共删除[7-9]。MTA是蛋氨酸挽救途径的中间体,对PRMT5有微弱的抑制作用。由于纯合子基因删除造成MTAP蛋白缺失,导致细胞代谢产物甲硫腺苷 (MTA) 在CDKN2A/MTAP共缺失的癌症细胞中积累。MTA水平升高会与激活辅因子S-腺苷甲硫氨酸 (SAM) 竞争结合PRMT5,产生PRMT5/MTA复合物[10]。据推测,结合并稳定PRMT5/MTA复合物的化合物将抑制无MTAP癌细胞中的PRMT5活性,同时在健康细胞中保持PRMT5的活性。另外研究表明,与表达MTAP的肿瘤相比,不表达MTAP蛋白的人类癌症表现出PRMT5活性的明显降低。由于PRMT5是一种细胞必需基因,在MTAP缺失的癌症中代谢产物MTA的积累使其对PRMT5的靶向治疗具有敏感性。
二、MTAP缺失的癌症的精确肿瘤学药物
MRTX1719是一种选择性结合并稳定催化失活的PRMT5/MTA复合物的小分子,与MTAP-WT细胞相比,它在MTA存在的情况下选择性抑制MTAP-del细胞中的PRMT5活性。发现MRTX1719的最初起点是4-(氨甲基) 酞嗪-1 (2H)-one fragment hit (F1),该片段是通过基于片段的线索发现 (FBLD) 方法鉴定的[11]。随后使用基于结构的药物设计 (SBDD) 的片段生长使MRTX1719得以发现 (图2)。MRTX1719在MTAP del肿瘤中显示出剂量依赖性抗肿瘤活性和对PRMT5依赖性SDMA修饰的抑制作用,可能是治疗MTAP缺失的癌症的一种潜在的精确肿瘤学药物。
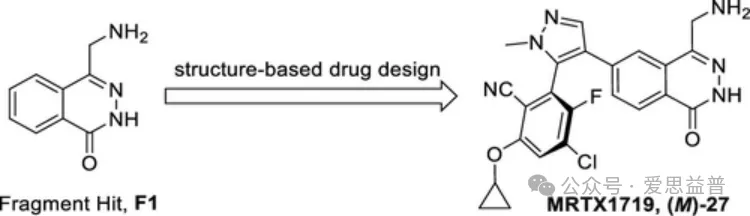
图2:使用SBDD和片段生长策略从片段命中F1中发现发展候选MRTX1719[11]。
三、PRMT5抑制剂的研究进展
PRMT5靶点药物尚未获批上市,目前有10款小分子药物处于临床阶段,两款待申报。适应症涵盖肿瘤、免疫系统和神经系统疾病。葛兰素史克的GSK-3326595处于二期临床,为进展最快的项目。国内外多家药企,如Prelude Therapeutics、Amgen、Mirati Therapeutics、Pfizer、GSK、石药集团、先声药业和圣和药业,正积极研发相关药物。
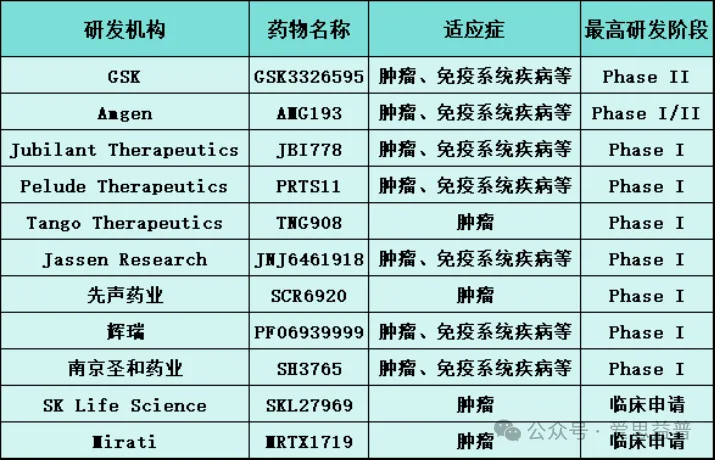
图3:进入临床的PRMT5抑制剂[12]
四、体内外模型助力MTAP缺失的癌症药物研发
近期爱思益普生物科技股份有限公司在人结直肠腺癌同基因细胞系对HCT116细胞敲除了MTAP,并测试得出了体外和体内疗效数据。
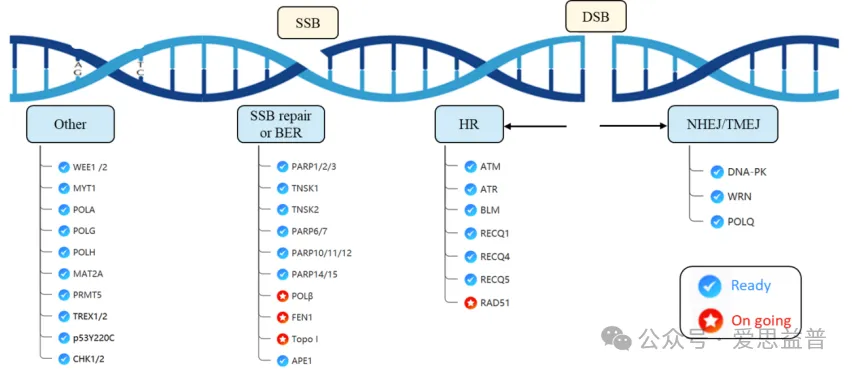
图4:DDR相关靶点
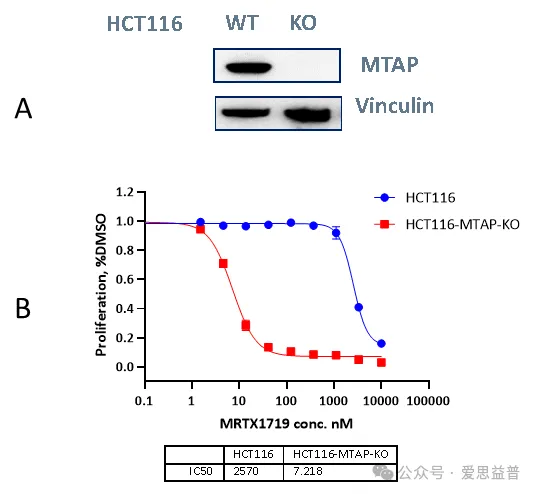
图5:HCT116 MTAP KO编辑株构建及体外验证: A.为Western blot验证MTAP的表达量结果。B.为细胞水平检测MRTX1719处理后细胞增殖情况。
成功获得HCT116 MTAP KO编辑株后,使用PRMT5抑制剂MRTX1719测试体内药效。观察肿瘤体积和小鼠体重变化,HCT116 MTAP KO模型组结果显示对于PRMT5靶点的化合物MRTX1719有效抑制了HCT116 MTAP KO肿瘤的生长。该模型已完成多轮成瘤测试,成瘤率100%。且模型成瘤均一,稳定性高。目前爱思益普使用此模型已为客户提供良好稳定的模型数据。
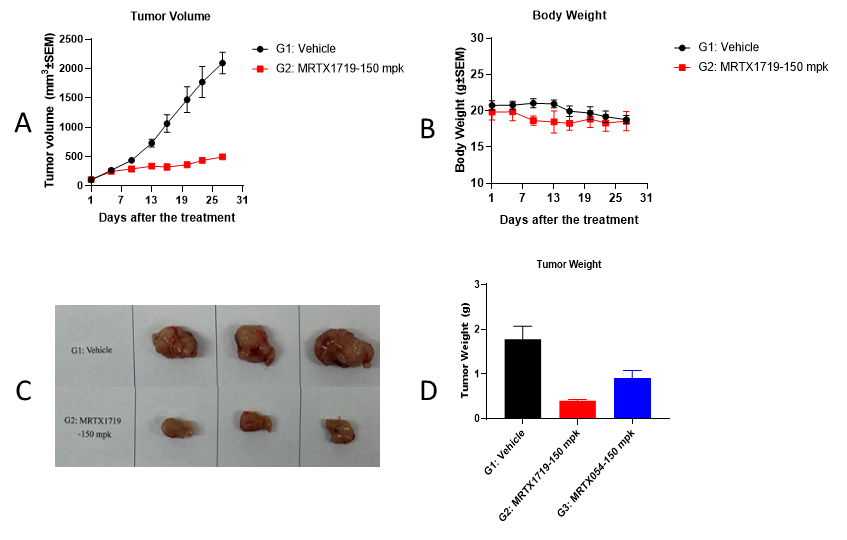
图6:HCT116 MTAP KO编辑株体内药效实验:A. 为HCT116 MTAP KO荷瘤小鼠不同给药测试后的瘤体积变化情况。B.为不同给药测试后的体重变化情况。C.为各组别肿瘤照片展示。D.图为肿瘤瘤重的变化情况。
1 Mulvaney KM, Blomquist C, Acharya N, Li R, Ranaghan MJ, O'Keefe M, Rodriguez DJ, Young MJ, Kesar D, Pal D, Stokes M, Nelson AJ, Jain SS, Yang A, Mullin-Bernstein Z, Columbus J, Bozal FK, Skepner A, Raymond D, LaRussa S, McKinney DC, Freyzon Y, Baidi Y, Porter D, Aguirre AJ, Ianari A, McMillan B, Sellers WR. Molecular basis for substrate recruitment to the PRMT5 methylosome. Mol Cell. 2021 Sep 2;81(17):3481-3495.e7. doi: 10.1016/j.molcel.2021.07.019. Epub 2021 Aug 5. PMID: 34358446; PMCID: PMC9016627.
2 Scaglione A, Patzig J, Liang J, Frawley R, Bok J, Mela A, Yattah C, Zhang J, Teo SX, Zhou T, Chen S, Bernstein E, Canoll P, Guccione E, Casaccia P. PRMT5-mediated regulation of developmental myelination. Nat Commun. 2018 Jul 19;9(1):2840. doi: 10.1038/s41467-018-04863-9. PMID: 30026560; PMCID: PMC6053423.
3 Pal S, Vishwanath SN, Erdjument-Bromage H, Tempst P, Sif S. Human SWI/SNF-associated PRMT5 methylates histone H3 arginine 8 and negatively regulates expression of ST7 and NM23 tumor suppressor genes. Mol Cell Biol. 2004 Nov;24(21):9630-45. doi: 10.1128/MCB.24.21.9630-9645.2004. PMID: 15485929; PMCID: PMC522266.
4 Migliori V, Müller J, Phalke S, Low D, Bezzi M, Mok WC, Sahu SK, Gunaratne J, Capasso P, Bassi C, Cecatiello V, De Marco A, Blackstock W, Kuznetsov V, Amati B, Mapelli M, Guccione E. Symmetric dimethylation of H3R2 is a newly identified histone mark that supports euchromatin maintenance. Nat Struct Mol Biol. 2012 Jan 8;19(2):136-44. doi: 10.1038/nsmb.2209. PMID: 22231400.
5 Xiao W, Chen X, Liu L, Shu Y, Zhang M, Zhong Y. Role of protein arginine methyltransferase 5 in human cancers. Biomed Pharmacother. 2019 Jun;114:108790. doi: 10.1016/j.biopha.2019.108790. Epub 2019 Mar 20. PMID: 30903920.
6 Abe Y, Sano T, Tanaka N. The Role of PRMT5 in Immuno-Oncology. Genes (Basel). 2023 Mar 9;14(3):678. doi: 10.3390/genes14030678. PMID: 36980950; PMCID: PMC10048035.
7 Kryukov GV, Wilson FH, Ruth JR, Paulk J, Tsherniak A, Marlow SE, Vazquez F, Weir BA, Fitzgerald ME, Tanaka M, Bielski CM, Scott JM, Dennis C, Cowley GS, Boehm JS, Root DE, Golub TR, Clish CB, Bradner JE, Hahn WC, Garraway LA. MTAP deletion confers enhanced dependency on the PRMT5 arginine methyltransferase in cancer cells. Science. 2016 Mar 11;351(6278):1214-8. doi: 10.1126/science.aad5214. Epub 2016 Feb 11. PMID: 26912360; PMCID: PMC4997612.
8 Marjon K, Cameron MJ, Quang P, Clasquin MF, Mandley E, Kunii K, McVay M, Choe S, Kernytsky A, Gross S, Konteatis Z, Murtie J, Blake ML, Travins J, Dorsch M, Biller SA, Marks KM. MTAP Deletions in Cancer Create Vulnerability to Targeting of the MAT2A/PRMT5/RIOK1 Axis. Cell Rep. 2016 Apr 19;15(3):574-587. doi: 10.1016/j.celrep.2016.03.043. Epub 2016 Apr 7. PMID: 27068473.
9 Mavrakis KJ, McDonald ER 3rd, Schlabach MR, Billy E, Hoffman GR, deWeck A, Ruddy DA, Venkatesan K, Yu J, McAllister G, Stump M, deBeaumont R, Ho S, Yue Y, Liu Y, Yan-Neale Y, Yang G, Lin F, Yin H, Gao H, Kipp DR, Zhao S, McNamara JT, Sprague ER, Zheng B, Lin Y, Cho YS, Gu J, Crawford K, Ciccone D, Vitari AC, Lai A, Capka V, Hurov K, Porter JA, Tallarico J, Mickanin C, Lees E, Pagliarini R, Keen N, Schmelzle T, Hofmann F, Stegmeier F, Sellers WR. Disordered methionine metabolism in MTAP/CDKN2A-deleted cancers leads to dependence on PRMT5. Science. 2016 Mar 11;351(6278):1208-13. doi: 10.1126/science.aad5944. Epub 2016 Feb 11. PMID: 26912361.
10 Mavrakis KJ, McDonald ER 3rd, Schlabach MR, Billy E, Hoffman GR, deWeck A, Ruddy DA, Venkatesan K, Yu J, McAllister G, Stump M, deBeaumont R, Ho S, Yue Y, Liu Y, Yan-Neale Y, Yang G, Lin F, Yin H, Gao H, Kipp DR, Zhao S, McNamara JT, Sprague ER, Zheng B, Lin Y, Cho YS, Gu J, Crawford K, Ciccone D, Vitari AC, Lai A, Capka V, Hurov K, Porter JA, Tallarico J, Mickanin C, Lees E, Pagliarini R, Keen N, Schmelzle T, Hofmann F, Stegmeier F, Sellers WR. Disordered methionine metabolism in MTAP/CDKN2A-deleted cancers leads to dependence on PRMT5. Science. 2016 Mar 11;351(6278):1208-13. doi: 10.1126/science.aad5944. Epub 2016 Feb 11. PMID: 26912361.
11 Smith CR, Aranda R, Bobinski TP, Briere DM, Burns AC, Christensen JG, Clarine J, Engstrom LD, Gunn RJ, Ivetac A, Jean-Baptiste R, Ketcham JM, Kobayashi M, Kuehler J, Kulyk S, Lawson JD, Moya K, Olson P, Rahbaek L, Thomas NC, Wang X, Waters LM, Marx MA. Fragment-Based Discovery of MRTX1719, a Synthetic Lethal Inhibitor of the PRMT5•MTA Complex for the Treatment of MTAP-Deleted Cancers. J Med Chem. 2022 Feb 10;65(3):1749-1766. doi: 10.1021/acs.jmedchem.1c01900. Epub 2022 Jan 18. PMID: 35041419.
12 数据来源网络公众号:缪可研 同写意Biotech 靶向PRMT5抑制剂的研究进展及未来方向。
